Introdução
A COVID-19 (doença coronavírus 2019) é a doença resultante da infecção pelo vírus SARS-CoV-2 (síndrome respiratória aguda grave coronavírus 2).1,2 Os coronavírus são uma família de vírus de RNA encontrados em animais, mas devido a mutações, tornaram-se patógenos humanos (Tabela 1). Os quatro coronavírus associados com doenças respiratórias leves em humanos são bem caracterizados e altamente endêmicos.
O surgimento dos patógenos SARS-CoV e MERS-CoV (síndrome respiratória do Oriente Médio coronavírus) criaram uma significante preocupação nos últimos anos, mas demonstraram uma transmissão limitada de humano para humano e os esforços para sua mitigação foram um sucesso. Por outro lado, o SARS-CoV-2 é altamente contagioso, é transmitido eficientemente de humano para humano e causou uma pandemia global. Esse vírus pode sobreviver por um longo período (horas a dias) sob muitas condições ambientais.
Tabela 1:
| Coronavírus | Identificação | Transmissão Humano para Humano | Taxa de Mortalidade (estimada) |
| SARS-CoV | 2003 | Baixa | 5-10% |
| MERS-CoV | 2012 | Baixa | ~30% |
| SARS-CoV-2 | 2019 | Significante | ~1-3% |
| 229E, NL63, OC43 e HKU1 | Décadas | Significante | Muito baixa Causa doença respiratória superior leve a moderada na maioria dos pacientes
|
Mecanismo da Infecção
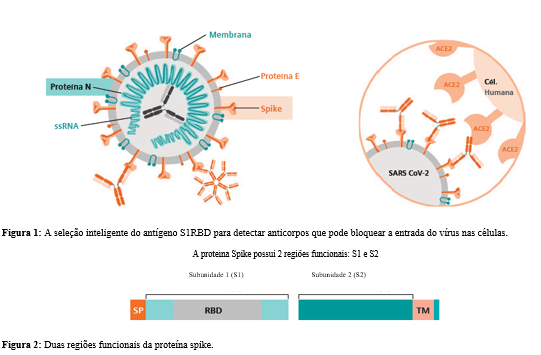
A estrutura do SARS-CoV-2 é mostrada na Figura 1. Trata-se de um vírus de RNA ligado à membrana com quatro proteínas estruturais principais: spike (S), envelope (E), membrana (M) e nucleocapsídeo (N).3 A proteína spike é uma glicoproteína transmembranar encontrada no exterior do vírus que reconhece e se liga ao receptor da enzima conversora de angiotensina 2 (ACE2) nas células humanas. Os receptores ACE2 são expressos em vários tipos de tecidos, incluindo os pulmões, o coração e o intestino.4
A proteína spike é dividida em duas regiões funcionais: S1 e S2 (Figura 2). A S1 contém uma região importante denominada domínio de ligação ao receptor (receptor-binding domain ou RBD). O RBD é uma porção da proteína spike que se liga diretamente ao receptor ACE2. Comparado aos outros coronavírus humanos, o SARS-CoV-2 RBD parece ter uma afinidade de ligação muito maior ao receptor humano.5,6 As comparações de sequência do SARS-CoV-2 RBD mostram uma diferença considerável em comparação aos outros coronavírus, incluindo o SARS-CoV, responsável pela maior afinidade. A alta afinidade de ligação contribui significativamente para o alto contágio.
Após a ligação inicial, uma conformação desencadeia a fusão mediada pela S2, permitindo que o vírus entre na célula e inicie a replicação. Como a proteína spike, particularmente a porção RBD, é essencial para a infecção, muitas vacinas em desenvolvimento a tem como alvo.7,8
A proteína N está localizada no interior do vírus e está estruturalmente ligada ao RNA. Funciona tanto no ciclo de replicações quanto em processos relacionados ao genoma viral. As proteínas virais M e E estão envolvidas na montagem e na maturação viral. Os testes sorológicos para SARS-CoV-2 tem como principal alvo a detecção de anticorpos dirigidos contra as proteínas S ou N.
Resposta do anticorpo ao SARS-CoV-2
A infecção desencadeia uma resposta do sistema imunológico ao hospedeiro, inata e adaptativa, que trabalham juntas para combater a infecção. Em alguns pacientes a doença se torna grave e está frequentemente associada a uma resposta inflamatória exacerbada (tempestade de citocinas) e hipercoagulabilidade. As razões para isso ainda precisam ser elucidadas, mas é uma característica patológica associada com doenças graves.9
Os anticorpos para SARS-CoV-2 tornam-se detectáveis em muitos pacientes por volta de 1 semana após o início dos sintomas. A maioria dos pacientes apresentam anticorpos detectáveis depois de 2 semanas, embora as diferenças nos ensaios utilizados possam afetar a detecção.10-13 É importante ressaltar que o aparecimento dos anticorpos não indica que a infecção foi curada, pois muitos pacientes soroconvertem IgM e IgG enquanto ainda há replicação viral ou durante um quadro agravado da doença.
Os testes desenvolvidos para a detecção dos anticorpos dirigidos as proteínas N e S (incluindo a S1 RBD) indicam uma resposta imune à infecção. Muitos dos testes de
anticorpos que chegaram inicialmente ao mercado tiveram problemas significativos de desempenho.14-17 Com a chegada de novos testes ao mercado é possível observar uma melhora no desempenho dos ensaios quanto a sensibilidade e especificidade.
Embora não tenham evidências de que os anticorpos para SARS-CoV-2 conferem resistência e/ou proteção a reinfecção após a recuperação, as evidências dos outros coronavírus sugerem que pode haver um certo nível de imunidade, pelo menos por alguns anos.18,19
Anticorpos neutralizantes e a imunidade ao SARS-CoV-2
Evidências indicam que pelo menos alguns anticorpos contra SARS-CoV-2 são neutralizantes, com base em dados in vitro. Os anticorpos neutralizantes são considerados os mais prováveis de conferir proteção. Além disso, estudos utilizando plasma convalescente de doadores positivos para anticorpos contra SARS-CoV-2 para tratamento de pacientes com a forma grave da doença mostraram potencial, embora não seja uma terapia recomendada atualmente. Os anticorpos neutralizantes são os supostos mediadores de eficácia nesse plasma.
Como nem todos os anticorpos são neutralizantes (muitos não são), será essencial determinar quais anticorpos específicos estão associados à proteção. Testes para aqueles anticorpos decorrentes de infecção resolvida ou de uma vacina bem-sucedida, quando ela for desenvolvida, podem permitir a designação da imunidade (ou o chamado “passaporte imunológico”). Também será importante entender se a proteção está associada aos níveis de anticorpos neutralizantes in vivo.
O Anticorpo para S1 RBD está associado à neutralização
Dado o papel essencial desempenhado pelo RBD no início da infecção, é razoável esperar que o anticorpo dirigido contra o RBD pode estar associado à imunidade. Em um estudo, dois anticorpos monoclonais dirigidos contra o RBD foram clonados a partir de células B em pacientes recuperados da COVID-19, e demonstraram neutralizar, mas não anticorpos para outros epítopos.21 Evidências adicionais apoiam o papel do anticorpo anti-RBD como neutralizante, juntamente com anticorpos para alguns outros epítopos na proteína spike.22-25 Isso é consistente com os dados que mostram que o RBD da S1 é o principal alvo dos anticorpos neutralizantes na SARS-CoV.26 Portanto, estratégias de vacinas que provocam um alto nível de anti-RBD podem ser eficazes. A avaliação quantitativa do anticorpo neutralizante pode ser útil, especialmente se os níveis diminuem com o tempo.
Em contraste ao S1 RBD, as evidências atuais de neutralização dos anticorpos contra a proteína N são limitadas ou inexistentes.
Tipos de teste de anticorpos na resposta imune à SARS-CoV-2
Três tipos principais de ensaios sorológicos foram desenvolvidos para testes de anticorpos em SARS-CoV-2. Testes para identificar IgM isoladamente, IgG isoladamente ou anticorpos total (pantípico) utilizando múltiplos formatos (fluxo lateral, ELISA, quimioluminescência automatizada, etc.), estão disponíveis comercialmente. Um número crescente de estudos apoia a incorporação do teste de anticorpos junto com o teste molecular em situações agudas (pacientes apresentando sinais e sintomas) para melhorar a detecção e apoiar a triagem do paciente, especialmente para pacientes que apresentam uma infecção posterior.27-29
Embora o teste do RNA viral possa confirmar a presença do vírus, ele não pode confirmar a ausência. Os motivos dos falsos negativos (FN) incluem a baixa carga viral na amostra coletada (swab nasofaríngeo, escarro etc.), questões pré-analíticas (técnica de coleta, transporte, armazenamento, extração de RNA etc.) e limitações do próprio teste (sensibilidade). Dados de estudos da COVID-19 indicam que a combinação dos resultados da sorologia com os testes moleculares pode melhorar a detecção em pacientes sintomáticos.27-29 No momento, o FDA recomendou que dois testes sorológicos separados que reconheçam anticorpos para diferentes antígenos (por exemplo, S e N) pudessem ser usados para melhorar o valor preditivo positivo (PPV).
Como o teste de anticorpos geralmente é mais acessível e pode ter um resultado rápido (o teste automatizado total Siemens Healthineers Atellica® SARS-CoV-2 leva apenas 10 minutos e relata a concordância percentual positiva (sensibilidade) e concordância percentual negativa (especificidade) > 99%), pacientes sintomáticos com teste de anticorpos positivo devem ser isolados até que testes e avaliações adicionais possam informar o diagnóstico e tratamento.
Os Testes de Anticorpos Totais (Pantípicos) podem ser mais sensíveis do que os de IgM ou IgG isoladamente
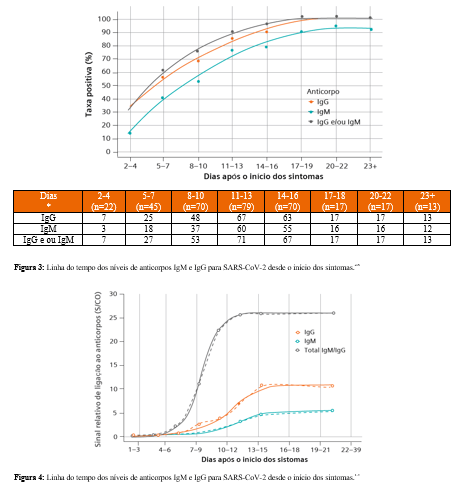
A soroconversão com SARS-CoV-2 exibe um padrão incomum (Figura 3). Ao contrário dos perfis típicos onde IgM pode estar presente por vários dias ou semanas antes que a IgG seja detectada, os estudos com o SARS-CoV-2 indicam que tanto a IgM quanto a IgG tornam-se rapidamente detectáveis, simultaneamente ou com apenas alguns dias de diferença.11,13 Devido ao rápido aparecimento de IgG, durante uma infecção ativa, um teste IgG positivo por si só não indica se o paciente se recuperou e não é mais uma pessoa potencialmente transmissora do vírus.
Embora os dados publicados mostrem que o uso de um teste de anticorpos total possa superar testes de IgM e IgG isoladamente na detecção precoce (Figura 4), a sensibilidade do teste pode influenciar significativamente o desempenho comparativo entre os ensaios. Serão necessários estudos que comparem ensaios quimioluminescentes altamente sensíveis, onde será possível entender as sensibilidades para testes de IgG e anticorpos totais para detecção precoce da resposta imune.
Referências:
- Wang L, et al. Review of the 2019 novel coronavirus (SARS-CoV-2) based on current evidence. International Journal of Antimicrobial Agents. Available from: https:// doi.org/10.1016/j.ijantimicag.2020.105948
- Guo YR, et al. The origin, transmission and clinical therapies on coronavirus disease 2019 (COVID-19) outbreak – an update on the status. Mil Med Res. 2020 Mar 13;7(1):11. doi: 10.1186/s40779-020-00240-0
- Astuti I, Ysrafil. Severe acute respiratory syndrome coronavirus 2 (SARSCoV-2): an overview of viral structure and host response. Diabetes & Metabolic Syndrome: Clinical Research & Reviews. 2020. Available from: https://doi.org/10.1016/j.dsx.2020.04.020
- Verdecchia P, et al. The pivotal link between ACE2 deficiency and SARS-CoV-2 infection. Eur J Intern Med. 2020 Apr 20. doi: 10.1016/j.ejim.2020.04.037
- Wang Q, et al. Structural and functional basis of SARS-CoV-2 entry by using human ACE2. Cell. 2020. Available from: https://doi.org/10.1016/j. cell.2020.03.045
- Shang J, et al. Cell entry mechanisms of SARS-CoV-2. Available from: www.pnas.org/cgi/doi/10.1073/ pnas.2003138117
- Chen WH, et al. The SARS-CoV-2 vaccine pipeline: an overview. Current Tropical Medicine Reports. Available from: https://doi.org/10.1007/s40475-020-00201-6
- Prompetchara E, et al. Immune responses in COVID-19 and potential vaccines: lessons learned from SARS and MERS epidemic. Asian Pac J Allergy Immunol. 2020;38:1-9. doi: 10.12932/AP-200220-077
- Nile SH, et al. COVID-19: pathogenesis, cytokine storm and therapeutic potential of interferons. Cytokine and Growth Factor Reviews. 2020. doi: https://doi.org/10.1016/j.cytogfr.2020.05.002
- To KK, et al. Temporal profiles of viral load in posterior oropharyngeal saliva samples and serum antibody responses during infection by SARS-CoV-2: an observational cohort study. Lancet Infect Dis. 2020;20:565-74. Available from: https://doi.org/10.1016/S1473-3099(20)30196-1
- Long QX, et al. Antibody responses to SARS-CoV-2 in patients with COVID-19. Nature Medicine. Available from: https://doi.org/10.1038/s41591-020-0897-1
- Infantino M, et al. Serological assays for SARS-CoV-2 infectious disease: benefits, limitations and perspectives. Isr Med Assoc J. 2020 Apr;22(4):203-10.
- Zhao J, et al. Antibody responses to SARS-CoV-2 in patients of novel coronavirus disease 2019. Clin Infect Dis. 2020 Mar 28. pii: ciaa344. doi: 10.1093/cid/ciaa344
- Lassaunière R, et al. Evaluation of nine commercial SARS-CoV-2 immunoassays. medRxiv. Available from: https://doi.org/10.1101/2020.04.09.20056325
- https://www.ucsf.edu/news/2020/04/417276/testing- tests-covid-19-antibody-assays-scrutinized-accuracy-ucsf-uc-berkeley. Accessed May 13, 2020.
- Abbasi J. The promise and peril of antibody testing for COVID-19. JAMA. Published online April 17, 2020. doi:10.1001/jama.2020.6170
- Whitman JD, et al. Test performance evaluate on of SARS-CoV-2 serological assays. medRxiv preprint. This version posted April 29, 2020. Available from: https://doi. org/10.1101/2020.04.25.20074856.
- Huang AT, et al. A systematic review of antibody mediated immunity to coronaviruses: antibody kinetics, correlates of protection, and association of antibody responses with severity of disease. medRxiv preprint. This version posted April 17, 2020. Available from: https://doi.org/10.1101/2020.04.14.20065771
- Lin Q, et al. Duration of serum neutralizing antibodies for SARS-CoV-2: lessons from SARS-CoV infection. Journal of Microbiology, Immunology and Infection. Available from: https://doi.org/10.1016/j.jmii.2020.03.015
- https://www.fda.gov/emergency-preparedness-and-response/coronavirus-disease-2019-covid-19/donate-covid-19-plasma. Accessed May 7, 2020.
- Chen X, et al. Cellular & Molecular Immunology. 2020 Apr. Available from: https://doi.org/10.1038/s41423-020-0426-7
- Wu F, et al. Neutralizing antibody responses to SARS-CoV-2 in a COVID-19 recovered patient cohort and their implications. medRxiv preprint. Available from: https://doi.org/10.1101/2020.03.30.20047365
- Jiang S, et al. Neutralizing antibodies against SARS-CoV-2 and other human coronaviruses. Trends Immunol. 2020 May;41(5):355-9. doi: 10.1016/j.it.2020.03.007. Epub 2020 Apr 2.
- Wang C, et al. A human monoclonal antibody blocking SARS-CoV-2 infection. Nature Communications. Available from: https://doi.org/10.1038/s41467-020-16256-y
- Wong SK, et al. A 193-amino acid fragment of the SARS coronavirus S protein efficiently binds angiotensin-converting enzyme 2. J Biol Chem. 2004;279:3197-201.
- Zhou G, Zhao Q. Perspectives on therapeutic neutralizing antibodies against the novel coronavirus SARS-CoV-2. Int J Biol Sci. 2020;16:1718-23.
- Kai-Wang To, et al. The Lancet Infectious Diseases. 2020 May. Available from: https://doi.org/10.1016/S1473-3099(20)30196-1
- Long Q, et al. Antibody responses to SARS-CoV-2 in patients with COVID-19. Nature Medicine. 2020 April. https://doi.org/10.1038/s41591-020-0897-1
- Lou B, et al. Serology characteristics of SARS-CoV-2 infection since the exposure and post symptoms onset. MedRxiv. 2020 March. Available from: https://www.medrxiv.org/content/10.1101/2020.03.23.20041707v1
Na Siemens Healthineers, nosso objetivo é permitir que os fornecedores de serviços e cuidados com a saúde aumentem o seu valor, capacitando-os em sua jornada para expandir a medicina de precisão, transformando a prestação de cuidados e melhorando a experiência do paciente, tudo possível pela digitalização dos cuidados com a saúde.
Estima-se que 5 milhões de pacientes beneficiam-se globalmente, todos os dias, de nossas tecnologias e serviços inovadores nas áreas de imagens terapêuticas, diagnósticos laboratoriais e medicina molecular, bem como saúde digital e serviços corporativos.
Somos uma empresa líder em tecnologia médica com mais de 120 anos de experiência e 18.000 patentes em todo o mundo. Com mais de 50.000 colegas dedicados em 75 países, continuaremos a inovar e moldar o futuro dos cuidados com a saúde.
Atellica e todas as marcas associadas são marcas comerciais da Siemens Healthcare Diagnostics Inc. ou de suas afiliadas. Todas as outras marcas comerciais e marcas são propriedade de seus respectivos proprietários.
A disponibilidade do produto pode variar de país para país e está sujeita a diversos requisitos regulatórios. Entre em contato com o seu representante local para verificar a disponibilidade.
[[Leia o artigo na íntegra na Revista Newslab 160]]