O ano de 2003 foi agourento para as doenças infecciosas emergentes. Um par de cepas de gripe mortais havia saltado de pássaros para humanos em Hong Kong e na Holanda. E um novo coronavírus estava se espalhando pelo mundo, causando uma doença misteriosa que ficou conhecida como síndrome respiratória aguda grave ou SARS. Muitos especialistas temiam estar assistindo ao início de uma pandemia global.
Felizmente, o pior cenário nunca se materializou. Mas foi um apelo próximo o suficiente para Robert Webster, uma das principais autoridades em gripe aviária, começar a incitar cientistas e legisladores a se prepararem para o próximo surto. Uma de suas principais recomendações: desenvolver e armazenar medicamentos que tenham como alvo uma ampla gama de patógenos virais 1 .
Os pesquisadores de drogas não atenderam ao seu apelo. Depois que a ameaça da SARS diminuiu, os juros evaporaram – e o mundo pagou o preço. “A comunidade científica realmente deveria ter desenvolvido antivirais universais contra a SARS”, diz Webster, agora membro emérito do St Jude Children’s Research Hospital em Memphis, Tennessee. “Então teríamos algo no estoque para o surgimento do COVID”, que é causado pelo SARS-CoV-2, um parente próximo do vírus responsável pelo SARS.
Outro tiro de alerta veio em 2012, quando a síndrome respiratória do Oriente Médio (MERS) – causada por outro parente do SARS-CoV-2 – começou a se espalhar por um punhado de países. Ainda assim, as prateleiras de drogas permaneceram praticamente vazias – um fato que Jay Bradner, presidente dos Institutos Novartis para Pesquisa BioMédica em Cambridge, Massachusetts, considera “lamentável”.
“Que vergonha”, diz ele sobre a indústria farmacêutica. “Podemos estar mais bem preparados.”
Além de um sucesso qualificado no remdesivir, uma terapia originalmente desenvolvida para tratar a hepatite C e o Ebola, praticamente não havia candidatos fortes a drogas antivirais para testar e implantar rapidamente contra a SARS-CoV-2. Os pesquisadores lamentam que não houvesse mais opções. “Precisamos de um arsenal”, disse Kara Carter, chefe de biologia de descoberta da empresa de biotecnologia Dewpoint Therapeutics em Boston, Massachusetts, e presidente da Sociedade Internacional de Pesquisa Antiviral.
Novas iniciativas para criar esse arsenal estão no horizonte. O Instituto Nacional de Saúde dos Estados Unidos (NIH), por exemplo, está planejando um grande programa para desenvolver terapêuticas contra as variantes do SARS-CoV-2 e outros vírus com potencial pandêmico. Uma nova coalizão apoiada pela indústria está visando os vírus da gripe e coronavírus. E alguns grupos esperam criar antivirais para patógenos mais remotos que representam um risco de pandemia.
Esses projetos não começarão do zero. O ano passado viu um bando de esforços de descoberta de medicamentos centrados na SARS-CoV-2. Mas com a indústria farmacêutica historicamente focada em apenas alguns vírus específicos – HIV e hepatite C, principalmente – encontrar agentes para combater ameaças conhecidas e imaginárias continua sendo uma tarefa difícil.
“Há muito trabalho a ser feito”, diz Nat Moorman, virologista da Universidade da Carolina do Norte (UNC) em Chapel Hill. Mas que escolha a comunidade científica tem? “Não queremos ter outro ano como 2020”, diz Moorman, “e não precisamos, se fizermos o trabalho com antecedência”.
Pronto para o trabalho
O remdesivir surgiu graças à prudência dos pesquisadores envolvidos no Centro de Desenvolvimento e Descoberta de Drogas Antivirais (AD3C), um projeto apoiado pelo NIH lançado há sete anos. Seu objetivo é rastrear as bibliotecas de drogas existentes para inibidores da gripe, coronavírus, alfavírus (como os responsáveis pelo chikungunya) e flavivírus (os patógenos por trás da dengue e do Zika, entre outros). Em 2017, membros do AD3C demonstraram o potencial anticoronavírus do remdesivir em modelos animais 2 . Na mesma época, testes realizados durante dois surtos de ebola na África mostraram que a droga era segura para as pessoas.
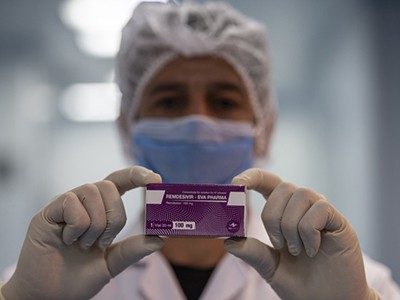
Técnicos de laboratório trabalham em remdesivir na Eva Pharma Facility no Cairo. Crédito: Amr Abdallah Dalsh / Reuters
Assim, quando o COVID-19 foi lançado, o remdesivir estava efetivamente pronto para funcionar. Ele poderia rapidamente entrar em testes em humanos para o novo coronavírus. Em um grande ensaio clínico controlado por placebo, executado durante três meses no início de 2020, os médicos demonstraram que a recuperação acelerada do medicamento entre pessoas hospitalizadas com COVID-19 3 . Mas a utilidade do remdesivir só vai até certo ponto. Alguns estudos clínicos não conseguiram confirmar se ele oferece aos pacientes qualquer benefício 4 . E o medicamento é caro, difícil de fabricar e deve ser administrado por via intravenosa em um hospital – todos atributos indesejáveis no meio de uma pandemia.
Outro medicamento antiviral que está prestes a ser aprovado pode resolver alguns desses problemas. O molnupiravir é uma opção de medicamento oral mais fácil de sintetizar que reduz a duração da infecciosidade entre as pessoas com COVID-19 sintomático. Os testes clínicos em estágio final estão em andamento.
Essa droga, também, foi estudada pela primeira vez 5 – pré-pandemia – por cientistas do AD3C, que também identificaram pistas promissoras contra alfavírus e flavivírus. De acordo com o líder do AD3C, Richard Whitley, um especialista em doenças infecciosas pediátricas da Universidade do Alabama em Birmingham, todos esses candidatos a drogas funcionam como blocos de construção genéticos falsos que obstruem a capacidade dos vírus de copiar seus genomas fielmente. Em vez de inserir as bases de RNA corretas durante a replicação, uma enzima viral chamada polimerase é induzida a incorporar derivados das drogas. As polimerases humanas não são enganadas, entretanto, apenas os vírus são afetados. (Medicamentos semelhantes são usados para tratar a hepatite B, HIV e vários outros vírus.)
Como os vírus em geral são fracos na detecção de erros genéticos, esses tipos de terapia – chamados de análogos de nucleosídeos – geralmente funcionam em famílias virais. Os medicamentos antivirais que se ligam diretamente às enzimas e bloqueiam sua função – ou seja, a grande maioria dos antivirais – não costumam ter uma atividade tão ampla. Em princípio, os cientistas poderiam desenvolver drogas que funcionassem em muitos vírus, indo atrás das regiões mais altamente conservadas das proteínas-alvo, diz Jasper Fuk-Woo Chan, um pesquisador emergente de doenças infecciosas da Universidade de Hong Kong. Mas, ele acrescenta, “tradicionalmente, sempre foi uma abordagem de ‘um bug, uma droga’”.
Essa filosofia tem servido bem para a indústria quando se trata de fazer novos medicamentos para HIV ou hepatite C. “Mas é comprovadamente ineficiente em termos de abordagem rápida de epidemias ou pandemias”, diz Chan.
Alvos complicados
De muitas maneiras, a estreita atividade dos antivirais existentes se resume à natureza dos próprios vírus. Outros tipos de patógenos – bactérias, fungos, parasitas – são mais facilmente contidos porque suas propriedades celulares oferecem uma abundância de alvos para a atividade de drogas. Pense na penicilina, que bloqueia a síntese da parede celular. Ou antifúngicos azólicos, que rompem a membrana celular.
Os vírus, com seus genomas compactos e falta de anatomia celular, oferecem muito menos alvos drogáveis. Adicione uma alta taxa de replicação – uma infecção típica de SARS-CoV-2, por exemplo, é pensada para produzir mais de um milhão de vírions por pessoa por dia 6 – juntamente com uma mutabilidade genética inerente, e não é de admirar que a maioria dos antivirais existentes provou ser inútil para COVID-19.
A plasticidade dos vírus significa que é improvável que um medicamento com atividade contra, digamos, o herpes faça uma diferença contra um coronavírus. Alejandro Chavez, bioengenheiro e pesquisador de drogas antivirais da Universidade de Columbia Irving Medical Center, em Nova York, duvida que alguém encontre um “inibidor divino que basicamente bloqueie tudo”.
“O que esperamos encontrar”, diz ele, “são inibidores que atuam, se você tiver muita sorte, em uma família inteira”. Isso faria do melhor cenário um inibidor de pan-coronavírus. Mas um objetivo mais razoável pode ser desenvolver um medicamento para um subconjunto de coronavírus, como os alfacoronavírus, que atualmente causam infecções não letais em humanos, e ter um medicamento diferente para betacoronavírus, o grupo responsável pela SARS, MERS e COVID-19 .
Uma vez que a linhagem viral é identificada, “os mesmos princípios da descoberta de drogas se aplicam”, diz Marnix Van Loock, chefe de patógenos emergentes na unidade global de saúde pública da Johnson & Johnson em Beerse, Bélgica. Como ele explica, os pesquisadores precisam encontrar ‘bolsões drogáveis’ na superfície de enzimas essenciais que são conservadas entre vírus relacionados e podem ser usadas para projetar moléculas ativas.
Isto é, pelo menos se o medicamento for dirigido ao próprio vírus. Em vez disso, alguns pesquisadores de drogas visam interferir nas vias humanas que uma ampla gama de vírus comanda para seus próprios fins. Jeffrey Glenn, por exemplo, está desenvolvendo uma droga que bloqueia uma enzima reguladora de gordura usada por muitos vírus para promover a entrada e replicação celular. Ao inibir essa enzima, “você priva o vírus de acesso a uma função do hospedeiro da qual ele depende”, diz Glenn, gastroenterologista e virologista molecular da Escola de Medicina da Universidade de Stanford, na Califórnia.
Outra estratégia antiviral dirigida pelo hospedeiro vem de dois ex-trainees de Glenn – Nam-Joon Cho, um cientista de materiais na Universidade Tecnológica de Nanyang em Cingapura, e Joshua Jackman, um engenheiro químico na Universidade Sungkyunkwan em Seul. Eles desenvolveram pequenas drogas peptídicas que fazem buracos nos invólucros lipídicos encontrados em torno dos vírus envelopados 7 . Esses lipídios vêm da superfície da membrana das células humanas. Mas os peptídeos penetram apenas nos lipídeos que envolvem os vírus, não nas células, por causa das diferenças no tamanho da estrutura da membrana e do quanto ela se dobra (consulte ‘As muitas maneiras de impedir os vírus’).
Crédito: Nik Spencer / Nature
Cho descreve o revestimento lipídico como o “denominador comum” de todos os vírus envelopados – um grupo que inclui flavivírus, alfavírus, coronavírus, filovírus, retrovírus e muito mais. Nenhum outro recurso compartilhado existe amplamente em todos esses vírus diversos, e é por isso que ele acha que os antivirais direcionados ao hospedeiro podem ter maior potencial como ferramentas de preparação para pandemias.
A biologia humana também oferece muito mais alvos potencialmente drogáveis do que os vírus. Além disso, os vírus são menos capazes de desenvolver resistência contra antivirais direcionados ao hospedeiro. Uma proteína viral pode precisar apenas de uma ou duas mutações para impedir a ligação da droga, por exemplo, enquanto uma terapia direcionada ao hospedeiro pode forçar o vírus a explorar processos celulares totalmente diferentes.
Alguns cientistas temem que adulterar as vias moleculares humanas possa causar efeitos colaterais indesejados – mas Shirit Einav, virologista e especialista em doenças infecciosas da Universidade de Stanford, acredita que as preocupações com a toxicidade são exageradas. “Tratamos todas as outras doenças visando uma função do hospedeiro”, diz ela, e as empresas farmacêuticas conseguem encontrar moléculas e regimes de dosagem que as pessoas podem tolerar. Então, por que os antivirais deveriam ser diferentes? Além do mais, ela acrescenta, “o tratamento de infecções agudas requer apenas vários dias de terapia” – não meses ou anos, como para doenças crônicas – “o que também ajuda a reduzir a toxicidade”.
Trabalho preparatório
Uma combinação de drogas direcionadas ao hospedeiro e de ação direta pode oferecer o melhor seguro contra futuras ameaças virais. Mas qualquer que seja a estratégia adotada pelos cientistas, os especialistas concordam que qualquer medicamento destinado à preparação para uma pandemia deve, no mínimo, ser totalmente testado em modelos animais e passar por alguns testes em voluntários humanos saudáveis. “Então, quando há uma pandemia, podemos implantá-los rapidamente na melhor faixa de dosagem para as pessoas”, diz a química Kelly Chibale, chefe do Centro de Desenvolvimento e Descoberta de Medicamentos da Universidade da Cidade do Cabo, África do Sul.
O objetivo seria aprovar e distribuir tal medicamento na janela crucial quando outros tipos de medicamentos de resposta rápida – como vacinas ou tratamentos com anticorpos – ainda não estiverem disponíveis.
Os desenvolvedores de medicamentos assumiram parte desse trabalho avançado após a SARS. Nos laboratórios La Jolla da empresa farmacêutica Pfizer, na Califórnia, por exemplo, os cientistas responderam ao surto de 2003 projetando uma molécula 8 que inibe uma proteína integrante da replicação do coronavírus, uma enzima conhecida como protease principal (M pro ), que corta longas cadeias de proteínas virais em suas partes funcionais.
Por cerca de seis meses, “foi um esforço muito intenso”, diz o químico Rob Kania, que liderou o projeto SARS da Pfizer. Mas as infecções logo desapareceram. E depois que os últimos casos de SARS foram relatados em 2004, a Pfizer e outras empresas que trabalhavam com medicamentos contra SARS arquivaram seus programas. Simplesmente não havia um mercado futuro para a terapia. Como o virologista da UNC Timothy Sheahan, que já trabalhou com produtos farmacêuticos, aponta: “É difícil convencer uma empresa a fazer um medicamento contra algo que não existe”.
A equipe de Kania nunca teve a chance de otimizar totalmente seu candidato principal para uso clínico, muito menos para testar a terapia em ratos ou em pessoas. Então, quando o SARS-CoV-2 apareceu e as análises genômicas revelaram que a proteína M pro do vírus era quase idêntica à do patógeno SARS original, ainda havia muitos ajustes químicos a serem feitos. Quando a droga, em uma forma ligeiramente diferente, estava pronta para teste em humanos 9 , a primeira onda da pandemia já havia diminuído e quase um milhão de pessoas morreram com a infecção em todo o mundo.
Essa droga, chamada PF-07304814, entrou em testes em setembro passado como um agente administrado por via intravenosa. Embora a pesquisa pudesse ter avançado ainda mais, pelo menos a Pfizer não estava começando do zero, diz Charlotte Allerton, chefe de design de medicamentos da empresa. Embora outros estejam trabalhando para bloquear o mesmo alvo, a Pfizer é a única fabricante de medicamentos com um inibidor experimental M pro em testes humanos hoje – dois deles, na verdade. Além de seu medicamento SARS reformulado, a Pfizer iniciou testes com um candidato oral diferente, o PF-07321332, no mês passado.
“Estou feliz por estarmos em uma posição de agir rápido e por termos feito o pré-trabalho? Sim ”, diz Allerton. “Eu gostaria de estar ainda mais longe e poder trazer opções de tratamento mais cedo? Absolutamente.”
Um alerta
As empresas que não tinham feito o mesmo tipo de trabalho braçal agora prometem não ser pegas de mãos vazias novamente. A pandemia foi “um alerta”, disse John Young, chefe global de doenças infecciosas da empresa farmacêutica Roche em Basel, Suíça. “É apenas uma questão de tempo antes do próximo”, diz ele, “e precisamos nos preparar como uma indústria”.
Para esse fim, os líderes da COVID R&D Alliance, uma coalizão de mais de 20 empresas de ciências biológicas e firmas de capital de risco que se reuniram no ano passado para combater a SARS-CoV-2 de forma colaborativa, estão agora lançando um projeto paralelo voltado para antivirais de espectro para coronavírus e vírus influenza. De acordo com Elliott Levy, chefe de pesquisa e estratégia de desenvolvimento e operações da Amgen em Thousand Oaks, Califórnia, que está liderando o esforço, o grupo planeja avançar cerca de 25 antivirais candidatos em estudos humanos iniciais e construir a infraestrutura de ensaios clínicos necessária para testes paralelos quando o próximo vírus mortal atacar.
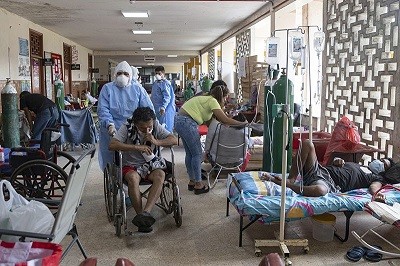
A adoção de um tratamento COVID não comprovado pela América Latina está dificultando os testes de medicamentos
O governo dos EUA tem ambições semelhantes. Os antivirais para coronavírus são a “tarefa número um”, diz o diretor do NIH, Francis Collins. Mas, disse ele à Nature , a iniciativa “certamente pretendia se estender a outras famílias virais, se os fundos estiverem disponíveis”.
Esforços complementares vêm do projeto Corona Accelerated P&D na Europa – um empreendimento de cinco anos de € 75,8 milhões (US $ 90,1 milhões). É voltado para encontrar medicamentos para a atual pandemia de COVID-19 e para futuros surtos de coronavírus. Moorman e outros pesquisadores da UNC, por meio de sua Rapidly Emerging Antiviral Drug Development Initiative, também esperam arrecadar US $ 500 milhões de governos, patrocinadores da indústria e fundações para desenvolver antivirais de amplo espectro e ação direta.
Enquanto isso, algumas grandes empresas farmacêuticas estão intensificando seus esforços internos. A Novartis, por exemplo, agora está otimizando um inibidor pan-coronavírus da enzima M pro . De acordo com John Tallarico, chefe de biologia química e terapêutica da Novartis, a empresa ainda está a pelo menos um ano de testes clínicos em humanos, momento em que o COVID-19 pode estar bem sob controle. No entanto, diz ele, a Novartis está empenhada em levar esse programa adiante.
Mas, diz Levy, “o nível de investimento da indústria hoje não é proporcional à ameaça” – é por isso que ele espera arrecadar cerca de US $ 1 bilhão apenas com as empresas farmacêuticas para o empreendimento spin-off de preparação para pandemia da COVID R&D Alliance. Fundos extras também podem vir de organizações sem fins lucrativos e outras partes interessadas, diz ele.
Andy Plump, presidente de pesquisa e desenvolvimento da Takeda Pharmaceutical em Cambridge, Massachusetts, e um dos líderes da aliança, está otimista quanto às chances de sucesso do programa. “No momento, você tem muita energia por trás disso porque existe o imediatismo do SARS-CoV-2”, diz Plump. Mas ele não quer que a apatia se instale novamente, como aconteceu depois da SARS e MERS. “Precisamos travar agora.”
FONTE: Nature 592 , 340-343 (2021)
doi: https://doi.org/10.1038/d41586-021-00958-4
Referências
- 1
Knobler, S. et al. (eds) Learning from SARS: Preparing for the Next Disease Outbreak: Workshop Summary (National Academies Press, 2004).
- 2
Sheahan, TP et al. Sci. Tradução Med. 9 , eaal3653 (2017).
- 3
Beigel, JH et al. N. Engl. J. Med. 383 , 1813-1826 (2020).
- 4
OMS Solidarity Trial Consortium N. Engl. J. Med. 384 , 497–511 (2021).
- 5
Sheahan, TP et al. Sci. Tradução Med. 12 , eabb5883 (2020).
- 6
Sender, R. et al. Pré-impressão em medRxiv https://doi.org/10.1101/2020.11.16.20232009 (2020).
- 7
Jackman, JA et al. Nature Mater. 17 , 971–977 (2018).
- 8
Hoffman, RL et al. J. Med. Chem. 63 , 12725–12747 (2020).
- 9
Boras, B. et al. Pré-impressão em bioRxiv https://doi.org/10.1101/2020.09.12.293498 (2021).