ARTIGO DE REVISÃO
AUTORES
Gavin I. Ellis, Neil C. Sheppard e James L. Riley
Nature Reviews Genetics (2021)
As células T são um componente chave do sistema imunológico adaptativo e podem ser subdivididas com base na função, expressão do co-receptor (CD4 ou CD8), tráfego, metabolismo e tempo de vida 5 , 6. As células T surgem de células-tronco hematopoéticas e amadurecem no timo. Durante este processo de desenvolvimento, as células T passam por um complexo programa de edição de genes, pelo qual segmentos gênicos dentro do locus do receptor de células T (TCR) são reorganizados aleatoriamente para gerar um TCR de especificidade única que permite que uma população de células T reconheça uma ampla gama de peptídeos apresentados por moléculas do complexo principal de histocompatibilidade (MHC). Quando um TCR reconhece o peptídeo cognato apresentado por meio de uma molécula de MHC em uma célula apresentadora de antígeno, um complexo de sinalização é recrutado para o TCR (sinal 1), que, quando acoplado a um ou mais sinais coestimuladores (sinal 2), inicia um segunda fase de desenvolvimento que leva à expansão do número de células T, diferenciação e, finalmente,
Alguns patógenos e tumores evitam habilmente a resposta das células T; por exemplo, o vírus Ebola interfere estericamente com as interações células T-MHC 7 e alguns tumores superexpressam o regulador imunológico PDL1, resultando em um limiar de sinalização mais alto para induzir o complemento total das funções efetoras das células T 8 . Ao usar ferramentas genéticas, os pesquisadores podem tirar proveito do que é conhecido sobre um patógeno ou tumor específico para gerar abordagens sintéticas para contornar os mecanismos de evasão e redirecionar as células T para um alvo desejado. Esta abordagem levou a curas completas e duráveis no caso de tumores que expressam CD19 9 (Quadro 1 ), gerando muitas outras terapias potenciais que estão em desenvolvimento para doenças infecciosas, autoimunidade e câncer.
Uma série de estratégias foram desenvolvidas para prolongar a função das células T, proteger os alogênicosAs células T da rejeição imunológica impedem que os vírus infectem as células T programadas para reconhecê-las e eliminá-las e aumentam as funções efetoras para eliminar um tumor ou patógeno específico. No entanto, até recentemente, o campo não tinha as ferramentas para implementar abordagens de terapia gênica complexas que aproveitassem ao máximo nosso conhecimento sobre a função das células T. Apenas alterações genéticas únicas de células T foram testadas, e as únicas terapias aprovadas pela FDA até agora, que tratam algumas leucemias e linfomas, usam células T projetadas para abrigar inserções genômicas colocadas aleatoriamente de um único gene sintético que redireciona as células T para matar. Engenharia adicional, além de redirecionar a célula T para um alvo, é provavelmente necessária para aumentar o número de indicações para as quais as células T geneticamente modificadas fornecem curas duráveis. Recentemente,10 , demonstrando viabilidade e segurança preliminar, inaugurando uma nova fase de terapia adotiva com células T envolvendo múltiplas manipulações genéticas. Embora este ensaio inicial tenha encontrado edições de genes fora do alvo e translocações cromossômicas, um ensaio de cultura in vitro de longo prazo usado antes da infusão não encontrou transformação de células T 10 . Para minimizar a edição de genes fora do alvo, uma variedade de melhorias nos sistemas de edição de genes CRISPR, incluindo edição de base, estão sendo desenvolvidos (revisado na ref. 11 ). Com uma caixa de ferramentas cada vez mais precisa e em expansão para a engenharia de células T, os pesquisadores agora estão ampliando o escopo das alterações das células T para curar uma variedade de doenças.
Aqui, revisamos por que as células T são células atraentes para engenharia genética, abordagens para manipular células T, como essas células T manipuladas estão sendo usadas para combater doenças crônicas e delinear como futuras estratégias de engenharia genética multifacetadas podem aumentar a segurança e eficácia. Nós nos concentramos na terapia do câncer e encaminhamos os leitores interessados em células T de engenharia para autoimunidade e doenças infecciosas para outras análises aprofundadas 12 , 13 .
Por que as células T são atraentes para engenharia?
Embora os tipos de células, como as células-tronco hematopoiéticas, as células B e os macrófagos tenham propriedades exclusivas que os tornam atraentes para terapias baseadas no sistema imunológico 14 , 15 , 16 , as células T estão na vanguarda deste novo pilar da medicina. Eles estão prontamente disponíveis por meio de uma punção venosa simples; sistemas de cultura e entrega compatíveis com boas práticas de fabricação (GMP) foram concebidos para expandir as células T ex vivo e reinfundi-las com segurança em pacientes 17 ; as lições aprendidas com o HIV geraram vetores de alta eficiência que transduzem prontamente as células T; As células T são células totalmente maduras que resistem à transformação oncogênica 18; e as células T modificadas têm o potencial de durar muito, com alguns estudos mostrando uma persistência de uma década 19 . Além disso, devido ao rearranjo genômico natural e edição que ocorre para gerar um TCR único, é tentador especular que eles estão bem equipados para executar e sobreviver a todas as formas de engenharia do genoma. Por último, a mobilidade e a gama funcional das células T as tornam excelentes agentes para a engenharia celular.
Fontes de células T
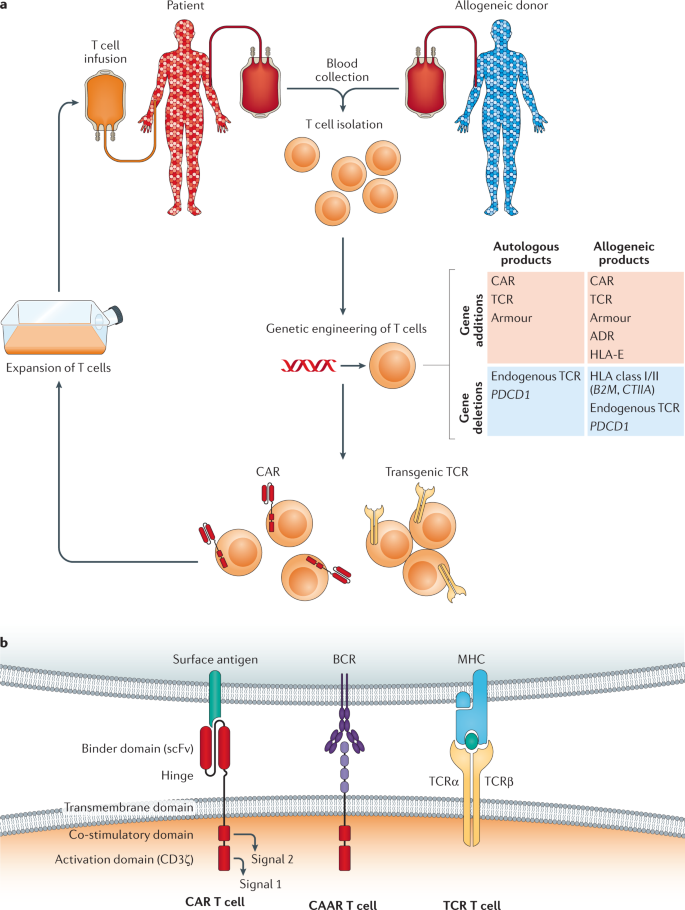
A primeira onda de terapias de células T adotivas por engenharia genética aprovadas usa células T autólogas em massa colhidas por aférese 20 , 21 , o que minimiza o risco de doença do enxerto contra hospedeiro (GVHD) e evita a depuração imunológica de células T terapêuticas 22 , 23 , 24 , 25 . Esta abordagem tem desvantagens notáveis, incluindo o tempo de resposta necessário para o processo de fabricação e logística individualizado (conhecido como o tempo “veia a veia”) durante o qual a doença de um paciente pode progredir 23 , 25 , o risco de falha de fabricação 23 , 25 e alto custo 26. Por essas razões, um esforço significativo está sendo despendido para desenvolver produtos de engenharia genética feitos de células T alogênicas como terapias ‘prontas para uso’. Três fontes de células T editadas por genes alogênicos estão sendo exploradas: doadores adultos saudáveis 27 , 28 , 29 , sangue do cordão umbilical 30 , 31 e células-tronco pluripotentes induzidas 32 , 33 .
Células T alogênicas geneticamente modificadas apresentam riscos e desvantagens únicos que não são encontrados com produtos de células T autólogas. Para combater esses desafios, o uso ideal de células T de terceiros pode exigir etapas adicionais de engenharia genética que não são necessárias para produtos autólogos (Fig. 1a ). De uma perspectiva de segurança, as células T alogênicas podem mediar GVHD 34 grave ou fatal , portanto, elas precisam ser obtidas de fontes de baixo risco, como doadores parcial ou totalmente HLA compatível 29 , 35 , células T específicas de vírus 28 ou cordão umbilical sangue 36 , 37 , ou o TCR endógeno deve ser excluído 27 , 38 , 39. Encontrar a combinação ideal de abordagens de engenharia genética para permitir que as células T alogênicas evitem a GVHD e sobrevivam em pacientes de diferentes tipos de HLA será a chave para estabelecer substitutos prontos para o uso de terapias celulares autólogas.
Tipos de células T projetadas
Células TCR transgênicas e células T CAR
As abordagens mais comuns para a engenharia de células T são a introdução de um TCR transgênico ou de um receptor de antígeno quimérico (CAR), que permite à célula T reconhecer um novo alvo (Fig. 1b ). A expansão e a transferência adotiva dessas células permitem a morte de células cancerosas ou infecciosas em massa. Ambas as abordagens têm seus pontos fortes e fracos. Os TCRs são capazes de acessar todo o proteoma da célula, mas são limitados pela necessidade de processamento de antígenos e apresentação de alvos peptídicos 17 . CARs ligam seus antígenos diretamente, e não estão limitados ao proteoma, mas se expandem para outras macromoléculas, como glicanos, que podem diferir marcadamente entre células normais e tumorais 40. No entanto, apenas antígenos acessíveis de superfície ou secretados podem atuar como alvos para os CARs 17 .
As células T TCR são predominantemente projetadas para expressar uma cadeia TCRα transgênica e uma cadeia TCRβ transgênica além ou no lugar de suas cadeias endógenas. O conceito surgiu da clonagem de TCRs de linfócitos infiltrantes de tumor, que poderiam redirecionar células T em massa para terem especificidade tumoral 41 . Na ligação de TCR transgênico a um peptídeo terapeuticamente relevante – MHC de interesse – por exemplo, o peptídeo 9-mer derivado dos aminoácidos 157-165 do antígeno de testículo de câncer altamente imunogênico NY-ESO-1, que é apresentado pelo HLA-A * 02: 01 (ref. 42 ) – a sinalização TCR natural ativa a função e expansão das células T.
O TCR endógeno pode limitar a eficácia das células T TCR de duas maneiras principais: por meio da competição pelo complexo CD3, reduzindo a expressão de TCR de superfície transgênica 43 , e por meio do pareamento incorreto entre as cadeias de TCR endógena e transgênica 43 . O pareamento incorreto da cadeia de TCR pode gerar novos TCRs com autoreatividade e alorreatividade 44 , reduz a quantidade do receptor transgênico desejado, limitando a potência 45 , 46 e apresenta um risco de toxicidade autoimune, que felizmente até agora foi observada apenas em camundongos 47 . Numerosas estratégias têm sido usadas para evitar o pareamento incorreto entre as cadeias de TCR endógena e transgênica, bem como para aumentar a expressão do TCR transgênico (revisado na ref. 48) e incluem a expressão equimolar de cadeias por meio de sequências de salto ribossomal 2A 49 ; modificações que facilitam a ligação intramolecular entre as cadeias α e β transgênicas, fundindo as cadeias ao CD3ζ; e nocaute da expressão de TCR endógeno via edição de nuclease 50 ou pequenos RNAs de interferência 51 . Recentemente, o primeiro ensaio clínico de células T TCR transferidas de forma adotiva com cadeias β e TCR endógenas editadas demonstrou segurança e viabilidade da abordagem 10 , com base em uma década de trabalho após o primeiro ensaio de células T TCR 52 .
As células CAR T abrigam um receptor transgênico personalizável que é uma quimera de um ‘domínio ligante’, tipicamente derivado de um anticorpo, com transmembrana derivada de células T e domínios de sinalização intracelular (Fig. 1b ). CARs aproveitam a requintada especificidade de ligação independente de MHC de anticorpos para ativar células T via TCR (sinal 1) e domínios de sinalização coestimuladores (sinal 2) 53 , 54 , 55 . O ajuste de afinidade de domínios ligantes e a seleção de domínios de sinalização são considerações importantes na terapia com células T CAR. Domínios ligantes de alta afinidade evitam o escape de tumor por células cancerígenas de antígeno 56 , enquanto domínios de baixa afinidade conferem citotoxicidade e proliferação aumentadas 57e pode poupar células normais que expressam níveis fisiológicos do antígeno alvo 56 . A escolha do domínio de sinalização intracelular deve corresponder ao caráter ideal da resposta imune desejada. Por exemplo, as células CAR T que expressam o domínio coestimulador ICOS secretam mais citocinas de células T auxiliares 17 em comparação com os domínios CD28 ou 4-1BB 54 .
Células T receptoras de autoanticorpos quiméricos (CAAR) (Fig. 1b ) são um subconjunto de células T CAR que amenizam doenças autoimunes mediadas por anticorpos, revertendo o paradigma de ligação anticorpo-proteína das células T CAR. Os CAARs contêm autoantígeno como seu domínio aglutinante extracelular, eliminando as células B secretoras de autoanticorpos ao se ligar a receptores de células B cognatas. As células T CAAR com um domínio ligante de desmogleína 3 matam células B patogênicas para melhorar o pênfigo em modelos animais da doença 58 , que se tornou a base para um ensaio clínico de fase I ( NCT04422912 ).
Células T regulatórias
As células T regulatórias (células T reg ) são células T CD4 + antiinflamatórias encarregadas de manter a homeostase imunológica com antígenos próprios e comensais. A transferência adotiva de células T reg é concebida para melhorar as pontuações de doenças autoimunes nas quais a escassez ou disfunção de células T reg contribui para a causa 59 , 60 , 61 ou para prevenir a doença onde a tolerância dominante falha em bloquear o início de uma resposta imune indesejada 12 . A transferência adotiva em escala clínica de células T reg expandidas in vitro não modificadas foi segura e diminuiu a incidência de GVHD após o transplante alogênico de medula óssea62 , abrindo caminho paracélulasT reg projetadas. AscélulasT reg são amplamente supressivas; a estimulação por meio de TCR ou CAR transgênicos pode suprimir simultaneamente uma variedade de tipos de células inflamatórias direcionadas a vários autoantígenos. AscélulasT reg parecem ter um limite inferior para o sinal 1, uma vez que os TCRs derivados de CD8 funcionam prontamente nas célulasT reg CD4 + , mas não nas célulasTCD4 + efetoras 63 . CélulasCAR T reg que reconhecem MHC classe I são protetoras em modelos animais de alotransplante e GVHD 64 , 65 , 66 , 67 , enquanto TCR T reg transgênicoas células foram projetadas para reconhecer antígenos de células β pancreáticas para o tratamento de diabetes mellitus tipo 1 68 , 69 .
A engenharia de células T reg se beneficiou do progresso na engenharia de células T efetoras, mas diferenças fundamentais na biologia entre os dois tipos de células apresentam desafios de design e fabricação exclusivos. Mesmo as modificações de células T mais bem-sucedidas devem ser avaliadas para tradução em células T reg in vitro e in vivo. Por exemplo, os domínios co-estimuladores 4-1BB e CD28, que são os principais contribuintes para a eficácia das células T CAR de Kymriah e Yescarta, sinalizam de forma diferente nas células T reg ; A coestimulação 4-1BB faz com que as células T reg percam a função supressora 70 , 71 . Além disso, a relativa escassez de T regas células no sangue periférico necessitam de classificação de GMP seguida por estimulação em série ex vivo, nenhuma das quais faz parte do processo de fabricação de células T CAR pró-inflamatórias 72 , 73 . A principal preocupação de segurança das células T reg modificadas é a perda de identidade das células T reg por conversão em células ex-FOXP3 secretoras de IL-17 ou secretoras de interferon γ em ambientes inflamatórios, o que acelera a progressão da doença 74 . As estratégias de mitigação incluem isolamento rigoroso de células T reg 72 , reforço da identidade de célula T reg por superexpressão de FOXP3 ou redirecionamento de células T efetoras para T reg editado pelo supressorcélulas ‘ao colocar FOXP3 endógeno sob o controle de um promotor ativo 75 .
Abordagens de engenharia genômica
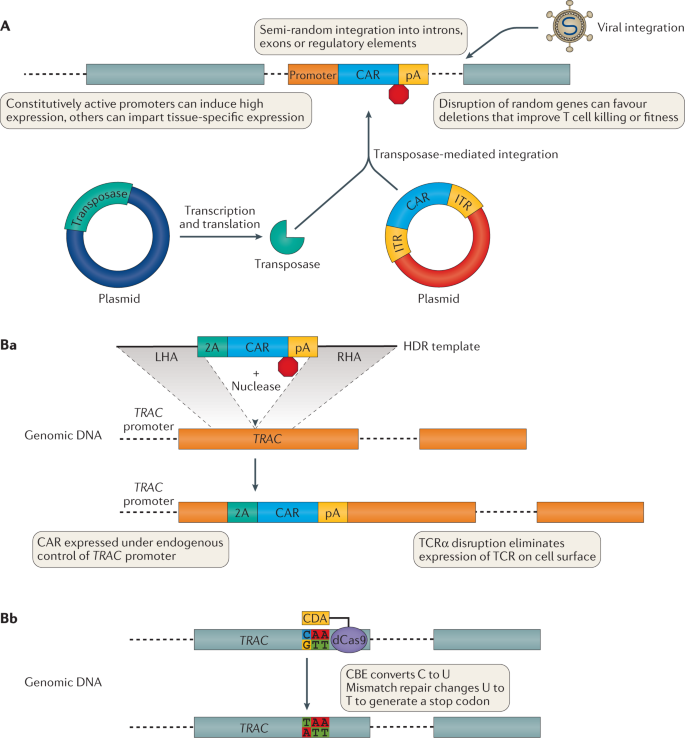
Em sua essência, a terapêutica com células T depende da capacidade de criar o genoma. As estratégias utilizadas podem ser amplamente estratificadas em tipos virais ou não virais e podem ter efeitos não específicos ou direcionados (Fig. 2 ). Conforme discutimos os prós e os contras das abordagens putativas, é importante perceber que um tamanho não serve para todos. A causa, gravidade, localização corporal e fisiopatologia da doença devem informar o desenho e a abordagem dos knock-ins, knockouts ou outras mutações genéticas pretendidos. À medida que a caixa de ferramentas de métodos para desenvolver DNA se expande, a fidelidade e a eficiência de cada método devem ser completamente caracterizadas em estudos pré-clínicos e clínicos para informar a abordagem ideal para cada tipo de desafio terapêutico.
A | Os vetores virais (parte superior) ou co-entrega de transposase e transposon (parte inferior) podem integrar transgenes no genoma de uma forma não direcionada. Ba | As quebras de fita dupla de DNA direcionado à nuclease na presença de DNA molde de reparo dirigido por homologia (HDR) facilita a integração do DNA molde em um locus genômico específico. Dependendo da concepção do molde e da localização das quebras de fita dupla de DNA, o transgene pode ser colocado sob o controle de um promotor endógeno e / ou pode eliminar a expressão de um gene ao qual se integra. Por exemplo, a integração de um transgene que expressa um receptor de antígeno quimérico (CAR) no locus TRAC , que codifica a região constante da cadeia α do receptor de células T (TCR), elimina a expressão de TCR endógeno. Bb| A citidina desaminase (CDA) ou adenina desaminase ligada a Cas9 cataliticamente inativo (‘morto’) (dCas9) forma um editor de base de citosina (CBE) ou editor de base de adenosina, respectivamente. A edição de bases pode reparar genes danificados ou gerar nocautes funcionais por meio da introdução de um novo códon de parada (mostrado) ou pela interrupção de pares de doador-aceitador de splice de RNA. 2A, péptido de salto ribossomal; ITR, repetição terminal invertida; LHA, braço esquerdo de homologia; pA, cauda poli (A); RHA, braço de homologia direito; TCR, receptor de células T.
Edição de genoma não direcionado
Entrega de gene viral
A transdução de vetor viral é um meio confiável de integração de um transgene no genoma da célula T (Fig. 2A ). O grande tamanho da embalagem permite a entrega de CARs ou TCRs, além de conjuntos multicistrônicos contendo transgenes adicionais para melhorar o comportamento do produto de células T. No entanto, provírus maior se correlaciona inversamente com o título, impondo um limite superior ao tamanho da carga 76 . A integração é semi-aleatória, com agrupamento de integração gammaretroviral baseado no vírus da leucemia murina de Moloney próximo aos locais de início da transcrição 77e integração lentiviral baseada em HIV mostrando uma propensão para genes ativos. A mutagênese por inserção de oncogenes ou genes supressores de tumor tem o potencial de causar transformação oncogênica por meio da desregulação desses genes. Embora os vetores gammaretrovirais tenham sido usados para os primeiros ensaios com células T CAR no final da década de 1990 78 , 79 , 80 , os vetores lentivirais se tornaram o vírus de escolha, devido à sua maior eficiência de transdução e expressão do transgene em células T 81 , 82 .
A sintonia da expressão do transgene viral pode ser modulada por meio do promotor e das sequências 3 ‘da região não traduzida que acompanham a região codificadora. Muitas vezes, CAR ou TCR de baixa afinidade e / ou baixa expressão do antígeno alvo podem tornar algumas células cancerosas invisíveis, necessitando de expressão máxima do receptor para efeito terapêutico suficiente. Promotores constitutivamente ativos combinados com regiões 3 ‘não traduzidas otimizadas 83 proporcionam expressão de transgene de alto nível estável em células T humanas primárias 81 , 84 . No entanto, a superexpressão de CAR pode levar à exaustão de células T 85e pode tornar o CAR mais reativo contra alvos de tecidos saudáveis de baixa expressão. Assim, uma cinética mais regulada pode ser favorável para permitir que a célula T CAR elimine tumores, ignore o tecido saudável e tenha força de ativação fisiológica e cinética. A incorporação de elementos reguladores dependentes de ativação ou específicos de tecido pode fornecer uma camada adicional de controle genético 86 .
Em contraste com os eventos de integração de genes oncogênicos, a mutagênese de inserção que causa superexpressão ou nocaute de outras proteínas em um produto terapêutico de células T é um fenômeno que está sendo explorado ativamente. A análise de células T transduzidas por vírus que são selecionadas por seu desenvolvimento no microambiente tumoral hipoglicêmico, hipóxico e carregado de citocinas poderia identificar genes que são vitais para a sobrevivência e função terapêutica entre tais pressões. Uma vez que o TCR exclusivo de cada célula T atua como um código de barras, o sequenciamento profundo do locus TCR pode caracterizar a resposta terapêutica como policlonal, pauciclonal ou monoclonal e rastrear uma população clonal funcional a partir do produto de infusão até o pico de resposta à manutenção de longo prazo. Em um paciente com leucemia linfocítica crônica que participa de um ensaio clínico com células T CAR CD19,87 . A análise do local de integração revelou a inserção do transgene CAR nolocus TET2 da metilcitosina dioxigenase, causando perda da função do gene. As células CAR T com knockdown de TET2 mostraram uma inclinação em direção a um fenótipo de memória central, aumento do crescimento in vitro e secreção de citocinas perturbada. Felizmente, esta expansão clonal maciça de células TET2 CAR / – retraiu para níveis de ponto de ajuste, ausente de transformação oncogênica 87 , cimentando o knockdown de TET2 como um candidato testável para knockdown intencional em terapia com células T CAR futuras. Análises moleculares semelhantes de respondedores e não respondedores irão descobrir outros processos fundamentais para a eficácia clínica.
Entrega de gene não viral
A entrega de genes não virais oferece um método alternativo de engenharia de células T livre do alto custo de produção e teste de segurança de células modificadas usando vetores virais. As células T são prontamente eletroporadas, permitindo que os complexos de DNA, RNA, proteínas e ribonucleoproteínas cruzem o plasma e as membranas nucleares. O mRNA transcrito in vitro pode ser introduzido em células T em repouso e ativadas, incitando a expressão transiente de uma proteína de interesse 88 . A magnitude e a persistência da expressão do transgene podem ser reguladas variando a quantidade de RNA eletroporado 88 , o comprimento da cauda poli (A) 89 e a inclusão de um tampão 5 ‘.
A co-transfecção de piggyBac ou transposase da Bela Adormecida com DNA contendo transgene aproveita ‘genes saltadores’ para integrar informação genética de forma não viral em células T modificadas 90 , 91 (Fig. 2A ). Tal como acontece com os vetores virais, o piggyBac prefere a integração nos genes e, portanto, traz o risco e a recompensa da mutagênese por inserção 92 , 93 . Em contraste, a Bela Adormecidaintegra genes favoravelmente para aplicação terapêutica de uma forma quase aleatória. No entanto, a toxicidade associada à entrega de DNA modelo e menor eficiência de transdução em comparação com vetores lentivirais limita a expansão de células T projetadas in vitro 94 , e deve-se ter cuidado para evitar a integração da própria transposase, levando à remobilização irrestrita do transgene. O desenvolvimento de novas formas de Sleeping Beauty 95 , 96 , juntamente com métodos para entrega de transposase e molde de transgene 97, continuam a apoiar a tradução clínica desta modalidade terapêutica. Os ensaios clínicos de terapia adotiva de células T CAR específicas de CD19 baseadas em transposon demonstraram a segurança e a viabilidade desta abordagem98 , 99 .
Edição de genoma direcionado
Uma nova safra de nucleases específicas do local concede a capacidade de selecionar onde um construto se integra ao genoma (Caixa 2 ). Cada método nesta classe compartilha um princípio básico – a capacidade de conduzir uma nuclease de DNA a uma região de interesse predeterminada. As quebras de fita dupla de DNA podem ser reparadas por processos de união de extremidades não homólogas ou de reparo dirigido por homologia (HDR). A junção final não homóloga repara quebras de fita dupla de DNA sem processamento final, ocasionalmente induzindo mutações de frameshift de inserção e deleção (indel), levando a códons de parada prematuros e nocaute projetado de expressão de proteína indesejada.
O HDR explora a homologia encontrada em cromátides irmãs não danificadas para resolver os danos. Esta via pode ser comandada por engenheiros celulares para entregar transgenes a um locus específico, entregando modelos de reparo de DNA contendo o transgene envolvido por braços de homologia específicos para ambos os lados da lesão de DNA (Fig. 2Ba ). Em contraste com a integração semi-aleatória com vetores virais ou transposases, a integração de um transgene em uma localização genômica precisa via HDR permite evitar a integração perto de um oncogene ou gene supressor de tumor, controle mais preciso do transgene por um promotor endógeno e / ou nocaute simultâneo de outra proteína. Uma vez que o único pré-requisito para HDR é uma quebra de fita dupla de DNA, múltiplas nucleases 85 , 100 , 101 ,102 foram usados para knock-ins mediados por HDR em células T. O DNA doador pode ser entregue às células T tanto pelo sorotipo 6 do vírus adeno-associado (refs 100 , 103 ) ou por eletroporação de DNA 104 , 105 . Para aumentar a segurança, o DNA pode ser inserido em um local de ‘porto seguro’ identificado como improvável de causar mutagênese de inserção 106 . Alternativamente, o modelo de HDR pode ser direcionado a um gene, gerando um benefício dois por um: nocaute de uma proteína de interesse indesejada e controle da expressão da proteína transgênica sob um novo promotor. Por exemplo, em células T TCR ou células T CAR, integração de um transgene no TRAC que codifica TCRαO locus simultaneamente elimina a expressão de TCR, aumentando a eficácia ao diminuir o pareamento cruzado com TCRα endógeno e coloca o receptor transgênico sob controle endógeno do promotor 85 TRAC (Fig. 2Ba ). Tal regulação melhora a função versus expressão constitutiva, reduzindo a exaustão de células T na ausência de sinalização tônica 85 . Essa abordagem destaca que controlar a expressão pode ser tão importante quanto o caráter do transgene. Na mesma linha, as integrações direcionadas podem ajudar a personalizar um produto celular para uma indicação de doença específica. Por exemplo, a inserção direcionada de CARs específicos para HIV no CCR5O locus torna as células T VIH CAR resultantes resistentes ao HIV, eliminando um co-receptor viral 107 .
Cada método de engenharia tem seus próprios benefícios e limitações (Tabela 1 ). Como muitos estão nos estágios iniciais de caracterização, o perfil geral de segurança de cada um ainda está sendo delineado. Um equilíbrio entre a edição no alvo e fora do alvo deve estar dentro da faixa terapêutica em que células suficientes são projetadas corretamente para ter um impacto na doença sem causar oncogênese ou disfunção devido à edição de um locus indesejado.
Abordagens de engenharia para aumentar a eficácia
O modo como uma célula T é projetada altera seu tráfico, função, sobrevivência e, em última análise, capacidade de curar doenças. Por exemplo, dentro de uma única estrutura CAR, construtos usando os domínios co-estimuladores CD28 ou 4-1BB têm diferenças marcantes, com CARs baseados em CD28 exibindo função efetora aprimorada e CARs baseados em 4-1BB tendo sobrevivência e expansão aprimoradas 24 , 81 , 108 , 109. Dado que mesmo mudanças sutis em como as células T são programadas podem ter efeitos dramáticos na função e persistência, programar corretamente uma célula T para enfrentar os desafios de um determinado cenário de doença é uma tarefa assustadora. No campo da oncologia, onde a exploração de células T geneticamente modificadas está concentrada, não há dois casos de uma determinada histologia de câncer idêntica em suas aberrações genéticas e epigenéticas, e os tumores adquirem mais heterogeneidade dentro de um paciente individual à medida que evoluem, complicando ainda mais o desafio de engenharia 8. De acordo com a heterogeneidade dos tumores, os modelos pré-clínicos e os primeiros estudos clínicos de terapias com células T criadas por engenharia genética revelaram uma panóplia de mecanismos que potencialmente contribuem para a eficácia insuficiente ou transitória. Tais percepções fornecem uma premissa para o projeto racional de terapias de células T geneticamente modificadas de ‘próxima geração’ equipadas por meio da adição (‘blindada’) ou da exclusão de fatores regulatórios específicos para superar os principais mecanismos de resistência imunológica de tumores, evitando a toxicidade (ver a seção intitulada Abordagens de engenharia para aumentar a segurança). À medida que formas mais avançadas de engenharia genética surgem, o objetivo final é programar as células T para atuar de uma forma mais discriminativa e dependente do contexto para aproveitar de forma otimizada a potência e a seletividade das células T contra o câncer.
Definindo o problema
Embora as barreiras à eficácia das terapias de células T projetadas possam ser categorizadas de várias maneiras, aqui as consideramos no cenário de oncologia usando uma estrutura bem conhecida do campo mais amplo de desenvolvimento de medicamentos, os ‘três pilares’ da sobrevivência de medicamentos candidatos em meados – teste clínico de fase 110 : (1) exposição de uma droga no local de ação, que para terapias com células T se refere ao processo ativo de tráfico para o tumor; (2) engajamento do alvo, que para as terapias com células T pode ser inferido como significando a diversidade nos níveis de expressão do antígeno alvo ou perda de antígenocomo resultado da edição imune; e (3) expressão da atividade farmacológica funcional, que neste contexto equivale à função sustentada da célula T terapêutica, uma vez que ela tenha engajado seu alvo, que é fortemente influenciada pelo microambiente tumoral. A estrutura de três pilares pode ser especialmente útil, dado que mesmo os ensaios de fase I das terapias CAR T ou TCR T são cuidadosamente examinados quanto a sinais de benefício clínico, e a aprovação regulatória foi baseada em estudos de braço único com menos de 100 pacientes 20 , 21 , semelhante ao tamanho de estudo de fase II típico para produtos farmacêuticos tradicionais. A Figura 3 resume algumas das estratégias específicas que foram usadas para aumentar a eficácia das células T manipuladas que são discutidas nas seções a seguir.
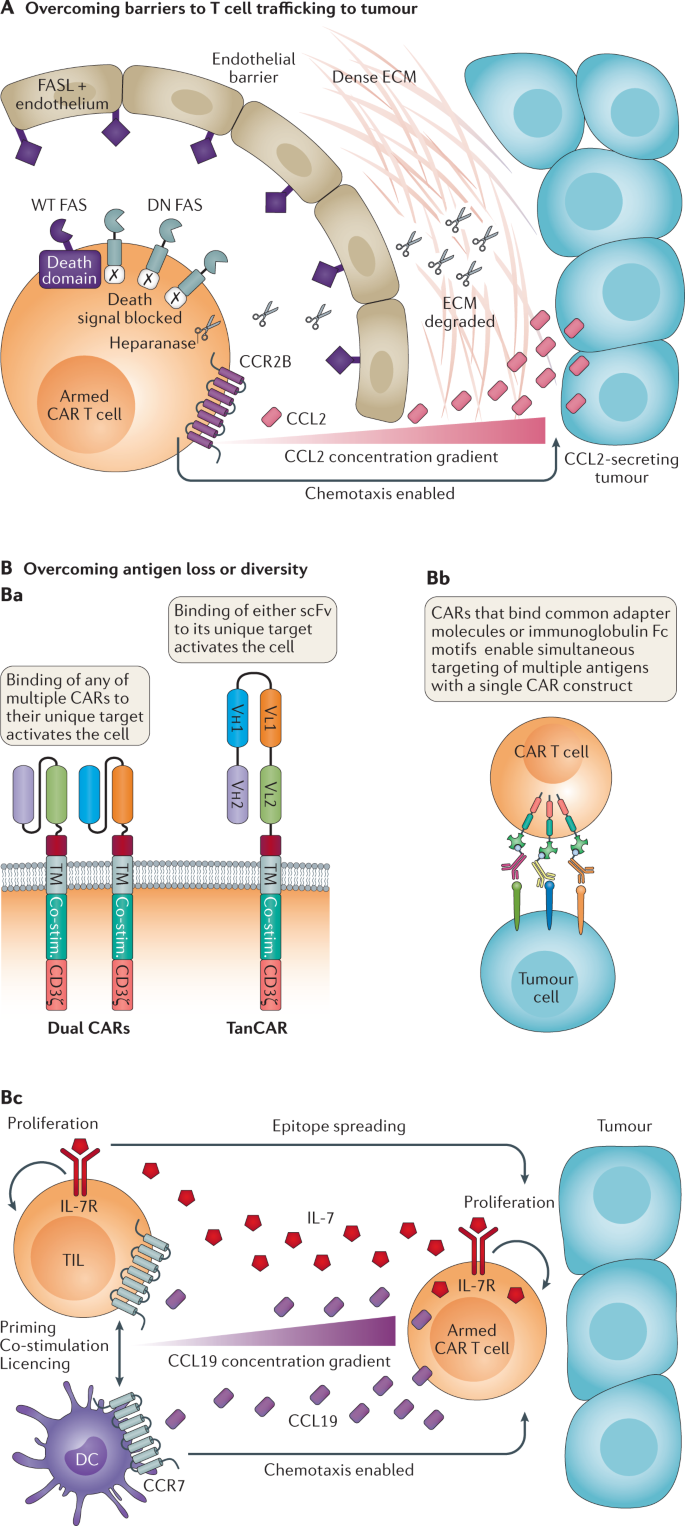
A | Superando barreiras ao tráfego de células T para o tumor. A adição de um receptor de quimiocina apropriado combinado para detectar quimiocinas liberadas pelo tumor alvo aumentou a infiltração de células T em modelos animais. A adição de um receptor FAS negativo dominante (DN) permitiu que as células T modificadas evitassem a indução de apoptose mediada pelo ligante FAS (FASL). Equipar as células T para secretar heparanase permitiu-lhes combater a densa matriz extracelular (ECM) de tumores em modelos pré-clínicos. B | Superar a perda ou diversidade de antígeno pode ser alcançada por transdução com dois ou mais receptores de antígenos quiméricos (CARs) (lógica de porta OR) ou via CARs em tandem (TanCARs) (painel Ba ), usando um CAR universal e ligantes de direcionamento de tumor separados (painel Bb) ou equipar células T para expressar fatores de crescimento e quimiocinas para aumentar a infiltração de tumores por células T e células dendríticas (DCs) (painel Bc ). Co-estim., Domínio co-estimulador; scFv, fragmento variável de cadeia única; TIL, linfócito infiltrante de tumor; TM, domínio transmembranar; WT, tipo selvagem.
Exposição no local de ação
O tráfico de células T é um processo complexo, ativo e de várias etapas que requer o engajamento de receptores de quimiocinas nas células T por quimiocinas liberadas no microambiente tumoral; a fixação, rolagem e parada de células T no endotélio ativado; e subsequente extravasamento e migração através da matriz extracelular do estroma do tecido 111 . Freqüentemente, há uma incompatibilidade entre os tipos de quimiocinas liberadas por tumores e os receptores de quimiocinas expressos por células T efetoras, resultando na diminuição da quimioatração 111 . Além disso, o endotélio dos vasos sanguíneos associados ao tumor é frequentemente anérgico à ativação por estímulos inflamatórios 111 , pouco conducente à fixação e extravasamento de células T 112, e tende a superexpressar o ligante FAS (FASL), desencadeando apoptose em células T efetoras 113 , 114 . Mesmo quando as células T efetoras superam esses obstáculos e chegam ao estroma tumoral, elas normalmente enfrentam uma matriz extracelular densa como uma barreira física adicional através da qual devem migrar 115 . A culminação das várias barreiras resulta em menos de 1% das células T transferidas de forma adotiva chegando com sucesso aos locais de ação para exercer um efeito farmacológico 116 , 117 .
Para melhorar o tráfego de células T criadas por engenharia genética para tumores, várias estratégias foram demonstradas em modelos pré-clínicos (Fig. 3A ). A engenharia das células T para expressar um receptor de quimiocina que responde às quimiocinas produzidas pelo tumor facilita a infiltração de células T nas lesões tumorais 118 . As células T equipadas com uma versão negativa dominante de FAS foram capazes de resistir à apoptose induzida por FASL 114 . Aqueles blindados para superexpressar heparanase foram capazes de digerir a densa matriz extracelular de tumores sólidos 119. Cada uma dessas abordagens mostrou benefício em modelos pré-clínicos, resultando em melhor controle do tumor, o que garante a exploração potencial em pacientes. No entanto, as diferenças entre os pacientes e mesmo entre os diferentes locais de metástase do tumor podem ser um obstáculo fundamental para a implementação.
Engajamento alvo
Para abordar a diversidade de antígenos intrínsecos de tumores 120 e a tendência de ambos os tumores hematológicos 121 e tumores sólidos 10 , 122 , 123 para sofrer perda de antígeno no tratamento com células T manipuladas, esforços para direcionar múltiplos antígenos ou para aumentar a resposta imune endógena promovendo espalhamento de epítopo foi proposto (Fig. 3B ).
Conceitualmente, talvez a abordagem mais direta para abordar a diversidade de antígenos ou escape seja um coquetel ou ‘pool CAR’ em que as células T CAR tradicionais de especificidade distinta são misturadas 124 . No entanto, para atender aos padrões de GMP, os pools CAR provavelmente exigirão a fabricação de cada componente separadamente antes da mistura em proporções definidas, multiplicando as considerações de custo. Alternativamente, as células T podem ser projetadas para expressar dois tipos de molécula CAR 125 ; isto é, um CAR duplo ou um CAR e um TCR 126 . Qualquer abordagem confere às células T a função de uma porta lógica booleana OR clássica, de modo que encontrar qualquer um dos antígenos é suficiente para ativar a célula T. Descobriu-se que os CARs duplos têm atividade superior em comparação com pools de CAR das mesmas especificidades individuais, além de serem mais fáceis de preparar 125 . Além disso, nosso grupo demonstrou recentemente que as células T CAR duplas transduzidas com dois CARs separados contendo um endodomínio CD28 / CD3ζ ou um endodomínio 4-1BB / CD3ζ melhoraram a função efetora, aumentaram a sobrevivência e aumentaram a expansão contra as células T CAR contendo um único CD28 / 4-1BB / CD3ζ CAR 53 .
Uma alternativa para expressar duas moléculas CAR separadas é o CAR biespecífico ou em tandem (TanCAR), em que ambos os ligantes são projetados em uma única molécula CAR 127 , 128 . Quando ambos os antígenos estão presentes, esta abordagem tem a vantagem de atividade superior em comparação com CARs duplos devido à formação de sinapses imunes aprimorada , e TanCARs requerem menos capacidade de codificação de nucleotídeos do que CARs duplos 127 , 128 . No entanto, TanCARs são inferiores aos pools de CAR ou CARs duplos quando o escape do antígeno em um antígeno já ocorreu 129 . Eles também têm a desvantagem de precisar determinar a ordem e o espaçamento ideais dos ligantes e o potencial de fragmento variável de cadeia única(scFv) ligantes para desemparelhar 130 . Expandindo o conceito de CAR duplo, um projeto de CAR T triespecífico também foi relatado no qual três construtos de CAR separados são entregues por meio de um lentivírus e expressos em uma única célula T; as células T CAR trivalentes foram capazes de reconhecer qualquer um dos três antígenos independentes 131 . Embora uma valência ainda maior possa ser possível com projetos futuros usando sistemas de entrega de genes com capacidade de codificação de nucleotídeos suficiente, uma limitação significativa ao aumento da valência pode ser a questão de agravar a toxicidade fora do tumor no alvo (discutida na seção intitulada Abordagens de engenharia para aumentar segurança) a níveis inaceitáveis.
Duas alternativas para abordar a diversidade de antígenos além de meramente aumentar a valência das células T geneticamente modificadas foram propostas: a célula T CAR “universal” emparelhada com uma biblioteca de módulos de direcionamento que podem ser infundidos separadamente e células T de engenharia para otimizar a indução e / ou recrutamento de uma resposta imune endógena, resultando na propagação do epítopo contra o tumor.
As células T CAR universais fazem uso de um único produto de células T que pode ser infundido em vários ambientes de doença, seguido pela infusão de frações de direcionamento distintas, onde a extremidade variável reconhece o antígeno tumoral selecionado e a extremidade constante é reconhecida pelo CAR universal. A forma mais simples desta plataforma toma emprestado o mecanismo de citotoxicidade celular dependente de anticorpo dependente de CD16 de células assassinas naturais, permitindo que células T que expressam um CAR baseado em CD16 sejam redirecionadas por anticorpos monoclonais terapêuticos existentes (mAbs) 132 . CARs universais alternativos podem ser redirecionados usando mAbs marcados ou conjugados com hapteno ou fragmentos de anticorpos, adaptadores biespecíficos 133 ou parceiros de ligação naturais, como estreptavidina-biotina (revisado na ref. 134) ou SpyTag-SpyCatcher 135 . Para implementar os sistemas CAR universais clinicamente, cada ligante de direcionamento precisa demonstrar farmacocinética, segurança e baixa imunogenicidade adequadas, e o grau em que as células T CAR universais podem persistir na ausência de direcionamento de um ligante precisará ser determinado.
O conhecimento da paisagem do antígeno no tumor de um determinado paciente, especialmente no que diz respeito à variação entre os locais metastáticos, provavelmente permanecerá limitado. Portanto, o conceito de células T de engenharia para promover a indução de respostas imunes endógenas é válido. Para este fim, as células CAR T projetadas para secretar IL-7 juntamente com CCL19 (conhecidas como células T CAR 7 × 19) 136 ou CCL21 (conhecidas como células T CAR 7 × 21) 137 foram relatadas (Fig. 3B ). IL-7 e CCL19 foram selecionados com base em sua importância na manutenção de zonas de células T em órgãos linfóides 136 , enquanto CCL21 foi selecionado devido à sua capacidade de atrair células T ingênuas e células dendríticas para zonas de células T, bem como por sua antiangiogênica efeitos 137. Os camundongos tratados com 7 × 19 células CAR T demonstraram um aumento nas células dendríticas e infiltração de células T tumorais com resolução melhorada de grandes tumores estabelecidos em comparação com células CAR T sozinhas 136 . A eficácia foi reduzida se as células T do hospedeiro foram eliminadas antes da terapia com células T CAR 7 × 19 e as células T endógenas CAR-negativas formaram respostas de memória ao tumor 136 . Enquanto isso, as células 7 × 21 CAR T superaram as células 7 × 19 CAR T e as células CAR T em vários modelos de camundongos, com evidências de células dendríticas intensificadas e infiltração de células T, redução da angiogênese e atividade contra tumores compostos por uma população mista de células que foram positivos ou negativos para o antígeno alvo 137 .
Com uma série de ensaios clínicos em andamento, ou já começando a produzir resultados 138 , 139 , 140 , testando várias estratégias para neutralizar a diversidade e o escape de antígenos, devemos aprender logo quais abordagens são mais apropriadas em determinados ambientes. Muitas malignidades de células B têm cargas mutacionais bastante baixas 141 e alta expressão de marcadores específicos de linhagem, como CD19, CD20 e CD22, que podem ser indicações ideais para células T CAR multitargeting. Na outra extremidade do espectro, tumores com alta carga de mutação, como carcinoma de pulmão de células não pequenas e melanoma 141, podem ser substratos melhores para abordagens que buscam quebrar a tolerância e induzir a propagação do epítopo.
Atingindo atividade farmacológica sustentada
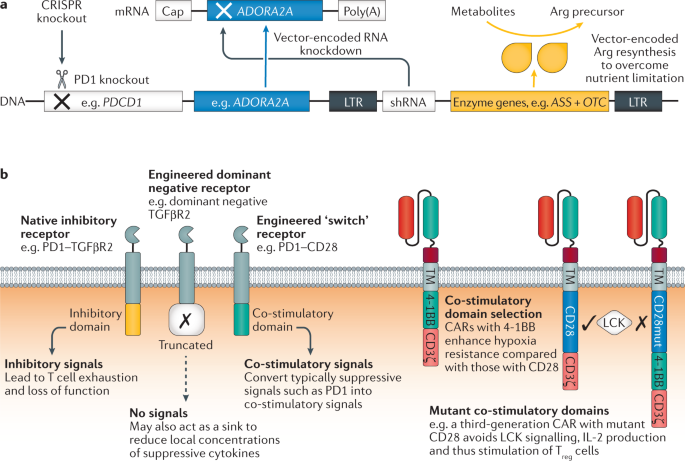
O microambiente tumoral supressor é uma barreira fundamental para a imunoterapia em geral e um desafio para estudar usando células T humanas manipuladas 142 . Numerosos mecanismos estão envolvidos, muitas vezes com crosstalk significativa, que incluem uma falta de nutrientes, hipóxia, a presença de metabólitos tóxicos, citocinas supressoras e pontos de verificação imunológicos e uma abundância de células supressivas estromais, mieloides e linfóides (revisado na ref. 143 ). A Figura 4 fornece exemplos de algumas das abordagens notáveis que foram implantadas para permitir que as células T de engenharia genética resistam aos efeitos do microambiente tumoral supressor e, assim, sustentem sua atividade farmacológica.
a | Muitas soluções de design potenciais estão disponíveis, incluindo a exclusão do gene (por exemplo, usando a edição do genoma CRISPR-Cas9 para eliminar PDCD1 ), interferência de RNA (por exemplo, knockdown do gene do receptor A 2A de adenosina ADORA2A para conferir resistência à adenosina) e adição de genes para permitir a auto-suficiência metabólica (por exemplo, adição de ASS e OTC , que codificam as enzimas argininosuccinato sintetase e ornitina transcarbamilase, respectivamente) ou que combatem pontos de verificação específicos e citocinas supressoras. b| Abordagens baseadas em receptor para resistir à supressão do microambiente tumoral (TME) incluem a expressão de uma forma negativa dominante de um receptor inibitório para agir como um sumidouro. Alternativamente, o domínio inibitório do receptor pode ser mudado para um domínio co-estimulador para mudar o sinal inibitório para um de ativação. As considerações de projeto do receptor de antígeno quimérico (CAR) incluem a escolha de domínios co-estimuladores; ambos os domínios co-estimuladores naturais e mutantes podem aumentar a capacidade da célula T modificada de sobreviver na TME supressora. Múltiplas estratégias podem ser usadas em paralelo e devem ser customizadas para os roadblocks de TME específicos encontrados. LTR, repetição terminal longa; shRNA, RNA em gancho curto; TM, domínio transmembranar; Célula T reg , célula T reguladora.
O surgimento de antagonistas de ponto de verificação PD1-PDL1 como uma classe principal de imunoterapias estimulou uma série de abordagens para lidar com esta via e pontos de verificação imunológicos semelhantes no cenário de células T geneticamente modificadas (consulte a seção intitulada Desafios na implementação de soluções). Notavelmente, essas abordagens incluíram os primeiros exemplos publicados de células T projetadas por CRISPR em pacientes, nos quais o gene para PD1, PDCD1 , foi deletado em células TCR específicas de NY-ESO-1 10 ou em células T em massa 144 (Fig. . 4a ).
O TGFβ também está emergindo como um fator imunossupressor chave em muitos tumores 145 . Para contrariar esta via, a abordagem do receptor negativo dominante tem sido usada (Fig. 4b ), por exemplo, em células T CAR direcionadas ao antígeno de membrana específico da próstata (PSMA), onde aumentou sua persistência e função in vitro e in vivo 146 . O receptor negativo dominante carece de um domínio de sinalização endógeno e, portanto, falha em propagar as vias de sinalização típicas a jusante do complexo do receptor, agindo como um sumidouro para a citocina e reduzindo a quantidade de sinalização supressiva de TGFβ para células T observadoras, bem como as Células T 147. Em um estudo clínico de linfócitos T citotóxicos específicos para o vírus Epstein-Barr (EBV) para o tratamento de linfoma de Hodgkin positivo para EBV, um paciente cujo tumor resistiu à terapia com linfócitos T citotóxicos não modificados obteve uma resposta objetiva na terapia subsequente com T citotóxico linfócitos que carregam o receptor dominante de TGFβ 148 . Com numerosos ensaios de células T geneticamente modificadas resistentes a TGFβ em andamento, podemos aprender em breve o grau em que a eficácia pode ser aumentada com segurança usando esta abordagem.
Além da infinidade de pontos de controle supressivos e citocinas, metabólitos como a adenosina, agindo por meio de receptores A 2A de adenosina , suprimem a atividade das células T. Para combater este desafio, as células CAR T foram projetadas para expressar uma molécula de RNA em gancho curto para desencadear a degradação do mRNA para o receptor de adenosina (Fig. 4a ). Esta abordagem teve sucesso na redução da expressão do receptor de adenosina por células T CAR e melhorou sua função in vitro e in vivo em modelos pré-clínicos 149 .
Células supressoras, incluindo células T reg , macrófagos do tipo M2 e células supressoras derivadas de mieloides, são reguladores chave da função das células T efetoras no microambiente tumoral 143 . As células T reg são um desafio especialmente pernicioso, uma vez que as células T efetoras ativadas secretam IL-2, promovendo a expansão das células T reg 150 . Para contrariar as células T reg , as células CAR T com CD28 e 4-1BB como moléculas co-estimuladoras foram projetadas com uma mutação no elemento CD28 impedindo o recrutamento da SRC quinase LCK, evitando assim a indução de IL-2 (Fig. 4b ) . Em modelos de camundongos, as células T CAR projetadas desta forma eram resistentes aos efeitos do T regcélulas 151 . Uma vez que os CARs de segunda geração com 4-1BB e CD3 sozinhos não foram testados, o estudo apoia principalmente um método para melhorar os CARs contendo CD28 em vez de demonstrar superioridade para construtos que utilizam domínios co-estimuladores alternativos.
Além das inúmeras células imunossupressoras, pontos de verificação e citocinas no microambiente tumoral, a demanda metabólica das próprias células tumorais, juntamente com a perfusão inadequada, contribui para a criação de um ambiente pobre em muitos nutrientes essenciais, bem como em oxigênio, representando desafios significativos para a função efetora sustentada de células T modificadas por engenharia genética 152 . Embora sejam possíveis muitas soluções de design que podem ajudar a contornar esses desafios, a escolha de domínios co-estimuladores para células T CAR é básica e impactante. Em comparação com a coestimulação de CD28, a coestimulação de 4-1BB resulta em capacidade respiratória de reserva mitocondrial aumentada em células T modificadas por gene e, portanto, uma capacidade aprimorada de funcionar em microambientes hipóxicos 153 (Fig. 4b ). Mecanismos mais complexos para aumentar a função das células T criadas por engenharia genética no microambiente tumoral incluem equipar as células T para expressar enzimas envolvidas na ressíntese do aminoácido crítico arginina 154 (Fig. 4a ). As células CAR T projetadas para expressar as enzimas argininossuccinato sintase e ornitina transcarbamilase eram autossuficientes em arginina e mantinham a função no microambiente tumoral, mostrando atividade aprimorada 154 .
Como os exemplos acima mostram, as contra-medidas que foram implantadas no ambiente pré-clínico ou clínico foram amplamente alcançadas por meio da simples adição ou exclusão de elementos regulatórios específicos. No entanto, dado que contramedidas específicas podem aumentar a potência das células T geneticamente modificadas para níveis potencialmente tóxicos, os cientistas estão cada vez mais buscando abordagens de engenharia mais complexas para combater a supressão imunológica em contextos específicos. Por exemplo, a citocina IL-12 é uma potente citocina imunoestimulante que é bastante tóxica quando administrada sistemicamente 155 . Quando expresso constitutivamente a partir de células T modificadas, impede a fabricação de um produto adequado ao desregular a expansão das células T e promover a apoptose 156. Em uma tentativa de aproveitar eficazmente a IL-12, uma cópia do gene de codificação foi adicionada às células T de TCR sob o controle de um promotor induzível por NFAT para ligar a expressão ao reconhecimento do antígeno tumoral. Embora esta abordagem tenha funcionado bem no ambiente pré-clínico 156 , um ensaio clínico testando a abordagem usando linfócitos infiltrantes de tumor ( NCT01236573 ) foi encerrado devido à toxicidade, sugerindo que o sistema NFAT estava muito furado ou a atividade do tumor no alvo. a infiltração de linfócitos e sua expansão em pacientes resultaram em níveis intoleráveis de produção de IL-12. Tal resultado ressalta a necessidade de um controle aprimorado das células T criadas por engenharia genética, especialmente quando blindadas para aumentar sua potência.
Desafios na implementação de soluções
Os desafios para a aplicação clínica bem-sucedida de estratégias de aumento de eficácia incluem encontrar uma indicação em que o mecanismo de resistência a ser tratado é uma barreira primária para a eficácia, selecionar uma contramedida idealmente projetada e estabelecer que a célula T aprimorada é suficientemente segura.
Embora muito do nosso conhecimento existente sobre contornar os mecanismos de resistência venha de modelos pré-clínicos e interrogatório de amostras de biópsia de pacientes de estudos clínicos anteriores, essas fontes sofrem com o viés potencial no que os investigadores escolheram estudar e como o mediram. As telas CRISPR têm sido usadas como uma maneira não tendenciosa de descobrir caminhos envolvidos na função aprimorada, estabilidade ou persistência de células T modificadas. Neste método, bibliotecas de RNAs guia direcionados a todo o genoma ou subconjuntos curados do genoma são incorporados em células T juntamente com Cas9 ou um Cas9 (dCas9) cataliticamente inativo (‘morto’) 157 . Após a aplicação de um método relevante de seleção – alta proliferação 158 , baixa expressão de FOXP3 159ou a presença no microambiente tumoral 160 , por exemplo – RNAs guia provirais são amplificados e sequenciados para descobrir alvos que representam nódulos importantes em vias relevantes para o processo selecionado. A incorporação de mais de um RNA guia por célula permite a identificação de coleções de alvos knockout que, de outra forma, seriam mascarados por epistasia ou complementaridade. Alternativamente, o knock-in CRISPR na presença de um pool de modelos de HDR pode selecionar rapidamente os transgenes que melhoram a função das células T CAR e TCR de uma maneira de alto rendimento. Por meio deste método, um receptor TGFβ – receptor de troca 4-1BB foi encontrado para aumentar a depuração mediada por células T TCR do melanoma 161. Ao descobrir células T funcionais que suportam as pressões seletivas do microambiente tumoral, as células T manipuladas podem ser projetadas para melhor corresponder a esse microambiente tumoral.
Uma vez que a principal via de resistência imunológica relevante para uma determinada terapia de células T geneticamente modificadas em um cenário de doença específico foi selecionada, a contramedida apropriada é necessária. Em geral, várias soluções de design podem ser propostas para lidar com qualquer desafio. Tomando a via PD1 como um exemplo, pode-se focar no nível genético em nocautear o gene PDCD1 10 ou derrubar sua expressão via interferência de RNA codificado por vetor 162 . Alternativamente, o PD1 endógeno pode ser deixado intocado e seus efeitos eliminados pela superexpressão de uma versão dominante negativa de PD1 (ref. 163 ), superexpressão de um receptor de ‘switch’ que converte o sinal em um sinal coestimulador 164 (Fig. 4b), desativando as vias de sinalização a jusante desencadeadas pela ligação PD1 165 ou equipando a célula T para secretar seus próprios agentes de bloqueio da via PD1, como anticorpos 166 ou PD1 solúvel (ref. 167 ). Além disso, além desses mecanismos que visam diretamente PD1, a sensibilidade das células T à disfunção mediada por PD1 depende de muitos outros fatores, que também podem ser modulados. Por exemplo, subconjuntos específicos de células T parecem ser intrinsecamente mais resistentes à supressão mediada por PD1 168 e exaustão em geral resultante de qualquer via de ponto de verificação pode ser direcionada por meio da neutralização dos fatores de transcrição envolvidos no estabelecimento ou manutenção da exaustão de células T, como TOX 169 , TCF1 (ref. 170) e membros da família NR4A 171 .
Uma vez que o projeto da contramedida para superar a resistência imunológica do tumor tenha sido estabelecido, o próximo obstáculo é estabelecer que a célula T produzida por engenharia genética resultante com sua potência aumentada será suficientemente segura e funcionará como previsto. No exemplo de PD1, uma célula T intrinsecamente resistente a PD1 pode ser indiscutivelmente mais segura do que uma que secreta um antagonista de PD1, já que o último também bloquearia PD1 em células T espectadoras. Também pode ser mais seguro do que o uso de um agente de ponto de verificação PD1 aprovado em combinação, novamente devido à restrição da resistência de PD1 à célula T terapêutica. No entanto, o uso de um anticorpo de ponto de verificação PD1 em combinação com uma célula T terapêutica pode ser controlado por meio de dosagem e retirada. Além disso, em um ensaio clínico recente de células TCR TCR nocaute de PD1, aquelas sem PD1 não persistiram bem10 , de acordo com as descobertas anteriores de que algum nível de sinalização de PD1 pode ser necessário para estabelecer a memória de células T 172 .
Como discutido acima, até agora, a engenharia de células T para maior eficácia envolve a exclusão ou adição bastante simples de genes específicos para neutralizar os obstáculos identificados para alcançar respostas clínicas profundas e sustentadas. A dificuldade tem sido em grande parte determinar quais barreiras são importantes e quais são secundárias. Muita ênfase no campo está em decifrar quais mudanças têm o maior impacto para uma doença específica. À medida que a capacidade de realizar várias alterações genéticas se torna mais comum, a ênfase mudará para quais mudanças se sinergizam para fornecer maior benefício terapêutico.
Abordagens de engenharia para aumentar a segurança
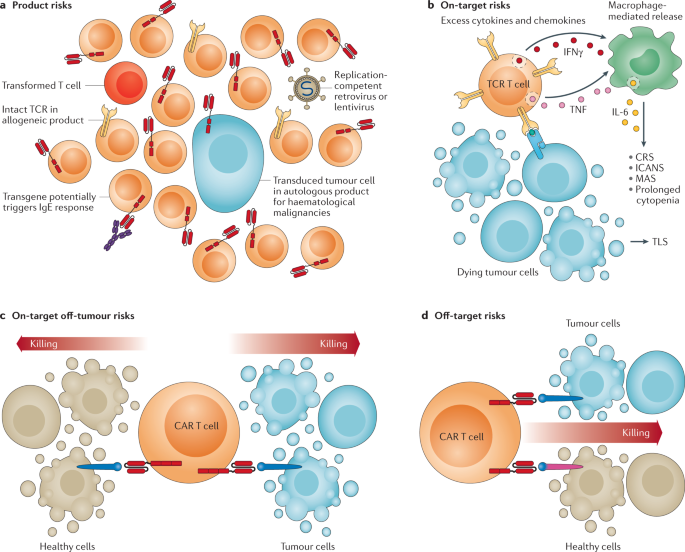
A capacidade das células T de proliferar, agir como serial killers de células-alvo positivas para o antígeno e orquestrar uma resposta imune mais ampla por meio da secreção de citocinas e quimiocinas é uma faca de dois gumes. Esses mecanismos tornam as células T um adversário adequado contra o câncer, mas também podem resultar em efeitos tóxicos graves ou fatais 173 , 174 . Os efeitos tóxicos associados às células T modificadas por engenharia genética foram investigados extensivamente 173 , 175 , 176 , 177 , 178 , 179 , 180 , 181 , 182e se enquadram em quatro categorias: (1) riscos do produto, (2) toxicidade no alvo, (3) toxicidade no alvo fora do tumor e (4) toxicidade fora do alvo (Fig. 5 ). Efeitos tóxicos significativos também podem resultar de drogas que fazem parte do regime de células T CAR ou TCR 173 , mas estão além do escopo desta revisão. O potencial para alcançar segurança desde o projeto por meio da engenharia genética aprimorada de produtos de células T é promissor. As várias soluções se enquadram em duas categorias, dependendo se permitem controle exógeno (ou seja, controle mediado por médico) ou são programadas endogenamente, permitindo que a célula T responda de forma autônoma para evitar ou reduzir a toxicidade (Fig. 6 ).
a | Os riscos do produto são as responsabilidades inerentes associadas ao produto fabricado, como contaminantes indesejados ou subprodutos do processo, incluindo vetores competentes de replicação, células tumorais residuais transformadas por receptor de antígeno quimérico (CAR), células T com danos no DNA que podem se tornar cancerígenas e células T alogênicas que escaparam da ablação do receptor de células T (TCR) e, portanto, representam um risco de doença do enxerto contra o hospedeiro. Esses riscos também incluem a potencial imunogenicidade da construção transgênica, que pode provocar reações à infusão. b| A toxicidade no alvo deriva de um excesso de morte de células alvo, resultando na síndrome de lise tumoral (TLS) ou de um excesso de produção de citocinas e quimiocinas pelas células T terapêuticas sozinhas ou em conjunto com células mieloides que resultam na síndrome de liberação de citocinas (CRS), síndrome de neurotoxicidade associada a células efetoras imunes (ICANS), síndrome de ativação macrofágica (MAS) ou citopenia prolongada. c | A toxicidade no alvo fora do tumor ocorre se o antígeno alvo também for encontrado nas células saudáveis em níveis suficientes para desencadear as células T terapêuticas. d | A toxicidade fora do alvo ocorre se o receptor imune transgênico apresenta reação cruzada com um antígeno encontrado em tecidos saudáveis. Interferão-γ de IFNγ; TNF, fator de necrose tumoral.
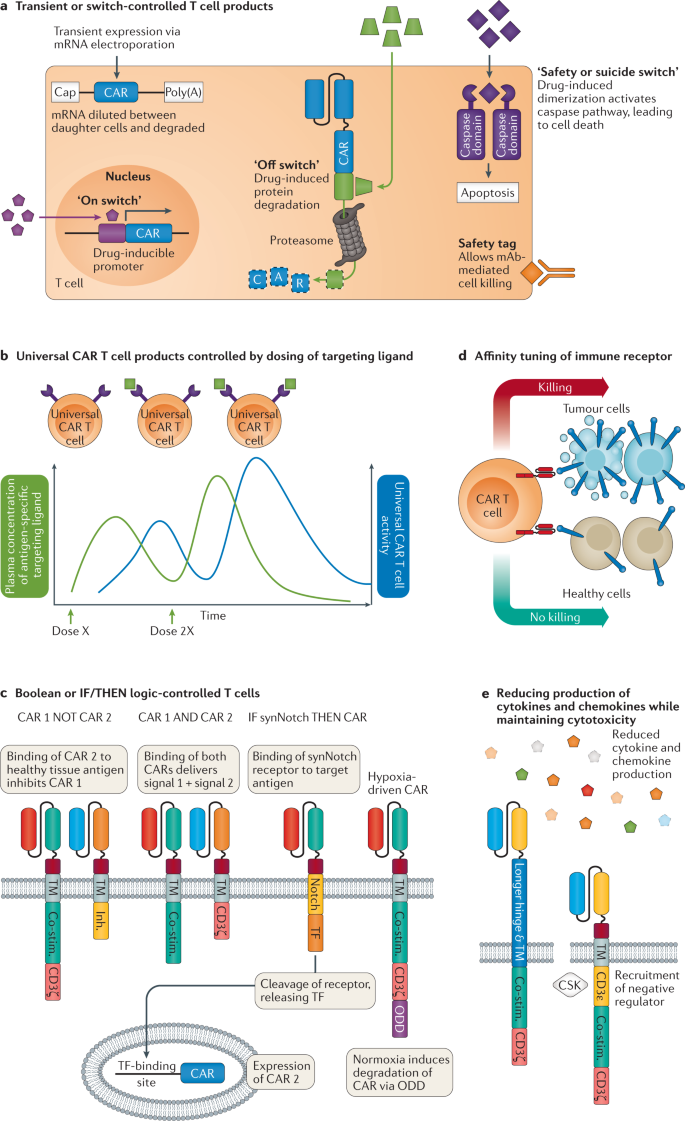
a | O controle exógeno de células T modificadas por engenharia genética pode ser alcançado por meio da entrega transitória do transgene usando eletroporação de mRNA ou por meio da aplicação de uma variedade de interruptores liga, desliga ou suicídio. O transgene pode ser ligado ou desligado no nível de transcrição ou via degradação de proteína induzida, ou a célula T terapêutica pode ser eliminada por um sistema de ativação de caspase ou por meio da inclusão de marcadores específicos reconhecidos por anticorpos monoclonais terapêuticos aprovados (mAbs) . b | O controle exógeno também pode ser alcançado por meio de um sistema de receptor de antígeno quimérico (CAR) “universal” no qual a infusão de ligantes de direcionamento específicos para antígenos separados redireciona as células T CAR para o alvo, enquanto a dose e o cronograma do ligante de direcionamento específico para antígeno podem ser modificado conforme necessário. c| O controle endógeno pode ser alcançado por meio de designs de CAR de tipo lógico booleano que requerem que as células CAR T reconheçam dois antígenos para ativação completa (porta E, por meio de um CAR dividido) ou inibam a ativação de células T CAR por meio de um segundo CAR inibitório (NÃO porta). O Notch sintético (SynNotch) e os sistemas indutíveis por hipóxia fornecem lógica ‘IF / THEN’ condicional para o controle endógeno da atividade das células T. No sistema SynNotch, o primeiro CAR é um receptor artificial do tipo Notch em que o reconhecimento do antígeno estimula a clivagem proteolítica de um fator de transcrição (TF), que por sua vez desencadeia a expressão de um segundo CAR ‘tradicional’ reconhecendo um antígeno separado, tornando a detecção do segundo antígeno dependente da primeira detecção do primeiro antígeno. No sistema induzível por hipóxia, o CAR inclui elementos sensores de oxigênio do fator 1α induzível por hipóxia,d | A sintonia de afinidade do receptor imune fornece outra forma de controle endógeno em que a afinidade é definida para permitir que a célula T terapêutica seja ativada por tumores que expressam níveis elevados do antígeno, mas não por tecidos saudáveis que expressam níveis baixos. e | Estender o domínio de dobradiça e transmembrana (TM) de um CAR permitiu a manutenção da citotoxicidade, mas uma redução significativa na produção de citocinas e quimiocinas e subsequente síndrome de liberação de citocinas e síndrome de neurotoxicidade associada a células efetoras imunes 210 . Da mesma forma, a engenharia de CARs para expressar o domínio CD3ε recrutou o regulador negativo CSK e resultou em uma sinalização mais transitória com citotoxicidade mantida, mas expressão reduzida de citocinas e quimiocinas 228. Co-estim., Domínio co-estimulador; Inh., Domínio inibitório; ODD, domínio de degradação dependente de oxigênio.
Células T controladas exogenamente
Produtos transitórios ou prontamente esgotados
Um método simples para limitar a duração da atividade das células geneticamente modificadas é entregar o transgene usando eletroporação de mRNA 183 (Fig. 6a ). Este método limita a atividade devido à meia-vida finita do transcrito do mRNA e sua diluição entre as células filhas, com infusões repetidas dadas para superar a persistência transitória 183 . No entanto, esta abordagem pode exigir a produção de grandes quantidades de células T terapêuticas para atender às demandas de infusões repetidas. Além disso, a entrega repetida de um produto de células T de mRNA CAR com base em um scFv murino provocou anafilaxia devido ao surgimento de anticorpos humanos anti-murinos da classe IgE 184 , criando assim um novo risco de produto.
Como uma alternativa aos produtos de células T modificados com meia-vida curta, etiquetas e interruptores de segurança ou suicídio são uma classe de solução de engenharia destinada a permitir o esgotamento rápido da célula T modificada por genes em caso de toxicidade inaceitável (Fig. 6a ) . As marcas de segurança compreendem antígenos 185 inteiros ou 186 truncados codificados ao lado do CAR ou TCR que são reconhecidos por terapias de mAb aprovadas, permitindo a depleção por mecanismos dependentes de Fc . No entanto, como os mAbs geralmente não penetram no sistema nervoso central, onde as células T terapêuticas podem precisar ser esgotadas 187, e os mecanismos dependentes de Fc podem agir muito lentamente, especialmente em pacientes com linfopenia, a exploração de interruptores suicidas é justificada. O switch de segurança da caspase 9 induzível (iCasp9) é ativado por uma pequena molécula, rimiducida, que dimeriza os domínios do switch iCasp9, levando à rápida indução da apoptose 188 . Embora possa ser possível ativar parcialmente o interruptor ou tag suicida e, assim, evitar a eliminação total da célula T modificada por genes, uma toxicidade grave emergente provavelmente exigirá intervenção rigorosa e, portanto, o esgotamento das células T modificadas caras, provavelmente deixando o paciente enfrentar a progressão da doença caso se recuperem da toxicidade aguda. Por essas razões, alternativas para chaves de segurança estão sendo exploradas.
Chaves liga e desliga
Os interruptores liga e desliga atuam regulando a transcrição, tradução ou estabilidade da proteína do CAR ou TCR ou, alternativamente, regulando a disponibilidade de coestimulação para promover a ativação e sobrevivência das células T (Fig. 6a ).
Para regular a atividade do transgene no nível de transcrição, interruptores indutíveis por drogas, como o sistema indutível por tetraciclina (Tet-On) 189 , 190 , 191 e o sistema indutível por doxiciclina 192 foram demonstrados. Esses sistemas são um tanto limitados pela expressão ‘vazada’ do transgene, pela perda bastante lenta de expressão na retirada do medicamento 189 e pela imunogenicidade de um sistema regulador de antibiótico derivado de bactérias.
A dimerização da proteína induzível por rimiducida também foi usada para criar um ‘switch on’ para células T terapêuticas por dimerização de um construto de ‘sinal 2’ compreendendo MYD88 e CD40 para fornecer coestimulação potente para células CAR T que foram projetadas para serem minimamente ativas sem coestimulação 193 . Para habilitar um interruptor de ativação e um interruptor de segurança na mesma célula terapêutica, um interruptor iCasp9 usando rapamicina como um dimerizador foi relatado 194 . Uma alternativa no design do interruptor faz uso de um CAR dividido, onde a dimerização é desencadeada por um análogo da rapamicina que age nos domínios de ligação à rapamicina 195 . Além da detecção de moléculas pequenas nos interruptores, um elemento responsivo à luz foi demonstrado na configuração de células T do CAR, em que uma luz azul estimula a expressão do CAR196 . Até agora, este sistema demonstrou funcionar apenas para células T CAR distribuídas localmente em tumores subcutâneos em camundongos e ciclos necessários de 12 h de indução de luz e, portanto, a aplicabilidade a massas viscerais e períodos de indução mais curtos ainda precisa ser demonstrada.
Para regular a atividade do transgene no nível da tradução e / ou turnover da proteína, foram desenvolvidos sistemas de ‘desligamento’. Nesses sistemas, o transgene é marcado de forma a permitir a degradação induzida por drogas por meio do sistema ubiquitina-proteassoma. Isto é conseguido através da dosagem com uma molécula quimera de direcionamento de proteólise (PROTAC) 197 ou ativando domínios de autodegradação com compostos de moléculas pequenas 198 , 199 .
Como alternativa aos interruptores de desligamento embutidos, o inibidor de tirosina quinase aprovado dasatinibe pode desligar as células T CAR ao inibir a sinalização 200 mediada por LCK . De fato, o perfil farmacocinético favorável do dasatinibe apoiou a titulação da dose para moderar a atividade das células T CAR, e os efeitos inibitórios foram rapidamente revertidos in vitro e in vivo quando o medicamento foi retirado 200 . Uma desvantagem potencial de usar um interruptor de desligamento não seletivo se aplicado regularmente ou por períodos mais longos pode ser a supressão da propagação do epítopo, que requer o sistema imunológico endógeno e é um fator desejado na imunoterapia em geral.
Células T CAR universais
Uma abordagem alternativa para permitir o controle exógeno sobre células T geneticamente modificadas e, simultaneamente, abordar a questão da perda de antígeno é o CAR universal acima mencionado que se liga a uma fração de direcionamento infundida separadamente. Para otimizar a segurança, a porção de direcionamento deve ter uma meia-vida limitada para permitir o controle da atividade das células T CAR universais pela dose e cronograma de dosagem do ligante de direcionamento (Fig. 6b ). Este requisito pode desfavorecer o sistema CD16 CAR plus mAb 132, dada a longa meia-vida dos mAbs.
Uma barreira para a aplicação de todas as plataformas de terapia com células T geneticamente modificadas controladas exogenamente será o desenvolvimento de diretrizes clínicas para regular a atividade das células T terapêuticas no paciente. Isso é especialmente desafiador, dada a falta de métodos para análise em tempo real de biomarcadores, como níveis de citocinas e células T, deixando o médico reagir a dados desatualizados.
Células T programadas endogenamente
Booleanas e portas lógicas IF / THEN
Na última década, surgiram os equivalentes biológicos das portas lógicas booleanas OR, AND e NOT (revisadas na ref. 201 ). A porta OR é projetada para evitar o escape de antígeno em vez de aumentar a especificidade 202 e foi discutido anteriormente, mas as portas AND e NOT foram projetadas com o aumento da especificidade do tumor em mente (Fig. 6c) No entanto, essas portas lógicas booleanas de células T têm suas desvantagens. Para a porta AND, em que ‘sinal 1’ (CD3ζ) e ‘sinal 2’ são divididos em CARs separados, o sinal 1 sozinho é suficiente para acionar a ativação da memória e subconjuntos de células T efetoras no produto de engenharia genética, enquanto a adição do sinal 2 aumenta a resposta e permite a ativação de células T naive. A perda de qualquer um dos antígenos alvo diminuirá a atividade do produto, aumentando o risco de escape do tumor. Para a porta NOT, em que um segundo CAR fornece um sinal supressor, é desafiador encontrar um alvo ideal associado a tecidos saudáveis que está ausente em tumores e projetar um sinal inibidor suficientemente potente para o NOT CAR 203. Essas limitações estimularam o projeto de um novo sistema lógico de proteínas e de circuitos genéticos mais avançados, como Notch sintético (SynNotch) e sistemas indutíveis por hipóxia.
O sistema de lógica de proteína é um verdadeiro sistema de lógica booleana que combina os requisitos de antígeno combinatório dos CARs de lógica booleana mencionados acima com o conceito de um sistema de célula T CAR universal que reconhece um ligante de direcionamento programado por lógica infundido separadamente. O sistema se baseia em switches de proteína gaiola-chave ortogonal de travamento dependente de colocalização sinteticamente projetados (co-LOCKR) 204 . Estes são projetados com lógica combinatória AND, OR e NOT em mente, de modo que após a ligação a uma célula alvo, eles passam por uma mudança conformacional para revelar uma tag a ser reconhecida por uma célula CAR T específica da tag apenas se as condições lógicas necessárias forem conheceu. O controle preciso da atividade das células T CAR foi demonstrado in vitro com este sistema 204, mas será vital estabelecer se os co-LOCKR switches, que são proteínas sintéticas não humanas, podem ser projetados com a farmacocinética necessária e baixa imunogenicidade para funcionar em pacientes, e continuará sendo um desafio encontrar alvos de antígenos apropriados para uso em componentes NOT lógicos, assim como era para os NOT CARs 203 anteriores .
Os sistemas CAR induzíveis por hipóxia e SynNotch são sistemas lógicos do tipo ‘IF / THEN’, em que um encontro com um antígeno ou condição específica induz a expressão funcional de um CAR para um segundo antígeno que é capaz de mediar a ativação completa de células T. O objetivo com esses sistemas é compartimentar a atividade de células T modificadas por engenharia genética para o tumor, reduzindo ou, de preferência, eliminando a atividade em tecidos saudáveis.
Para o sistema SynNotch, foi demonstrado que a toxicidade fora do tumor no alvo poderia ser evitada em modelos animais, desde que as células saudáveis que expressam o alvo do segundo CAR ‘tradicional’ não estivessem co-localizadas com o tumor 205 , 206 . Onde as células saudáveis e tumorais foram co-localizadas, uma vez preparadas pelo SynNotch CAR, as células T geneticamente modificadas foram capazes de matar tecidos tumorais e saudáveis com antígeno-positivos semelhantes a 205 , o que é uma desvantagem deste tipo de sistema que precisará de mais atenção . Além disso, os sistemas SynNotch atuais são limitados pelo uso de sequências imunogênicas de origem não humana, potencialmente limitando a persistência do produto no paciente.
Um sistema de expressão condicional totalmente humano alternativo liga a expressão do CAR à hipóxia, incluindo elementos do subdomínio sensível ao oxigênio de HIF1α na molécula do CAR 207 . Com o uso deste sistema, verificou-se que a expressão do CAR pode ser induzida por hipóxia e caiu 80% em 2 h quando a normóxia foi restaurada. O CAR resultante mostrou um diferencial dependente de hipóxia significativo na citotoxicidade em relação às células-alvo, embora essa mudança não seja binária 207 . Estudos futuros podem determinar se tais projetos limitam suficientemente a toxicidade fora do tumor no alvo, concentrando a ativação de células T em ambientes hipóxicos comuns a tumores sólidos.
Abordagens alternativas
Abordagens alternativas para sistemas com barreira lógica ou indutíveis incluem o ajuste da expressão ou afinidade do receptor transgênico, ou modulação de sua função alterando o comprimento do ligante entre os domínios de ligação ao antígeno e transmembrana (Fig. 6d , e ). Para abordagens que modulam a expressão ou afinidade do receptor imune, o objetivo final é calibrar o receptor imune para reconhecer densidades de antígeno típicas em células tumorais, poupando células saudáveis, com a possibilidade de também reduzir ou evitar a sinalização tônica, o que é prejudicial para Função e persistência das células T 85 . A expressão de transgenes pode ser regulada no nível de estabilidade do transcrito de mRNA por meio da inclusão de elementos de resposta a microRNA 208ou ao nível da proteína por inclusão de marcadores desestabilizadores conhecidos como ‘degrons’ 209 . Até agora, os sistemas de modelo de trabalho para ambas as abordagens foram descritos, e sua aplicação a células T CAR ou células T TCR está pendente. Foi demonstrado que o ajuste de afinidade do domínio de ligação ao antígeno permite que as células T modificadas com genes evitem a ativação por baixos níveis de antígeno em células saudáveis, enquanto retêm a atividade antitumoral 56 . Finalmente, a alteração do comprimento da dobradiça em uma célula T CD19 CAR foi mostrada tanto em modelos pré-clínicos quanto na clínica para desacoplar a eficácia da síndrome de liberação de citocina e da síndrome de neurotoxicidade associada a células efetoras imunes, reduzindo a produção de citocina enquanto mantém a citotoxicidade 210. Iterações e melhorias no projeto do receptor imunológico usando os conceitos de lógica de bloqueio, indução condicional e / ou expressão ajustada ou afinidade de ligação provavelmente aumentarão a segurança inerente de terapias de células T geneticamente modificadas, simplificando assim o gerenciamento de toxicidade.
Considerações finais
A engenharia genética de células T está abrindo novos caminhos para tratar uma ampla gama de doenças. Abordagens bem-sucedidas até o momento dependem da expressão constitutiva de uma única proteína. Para atingir o potencial total das células T modificadas, numerosas alterações genéticas provavelmente serão necessárias. Além disso, as abordagens de engenharia que permitem que as células T se adaptem a vários desafios simultaneamente, como a adaptação ao escape do antígeno, ambientes com nutrientes pobres e exaustão das células T, provavelmente serão necessárias para permitir resultados clínicos bem-sucedidos e duráveis. A facilidade de engenharia e o impressionante conjunto de funções de resposta pró-imune e anti-imune das células T abre possibilidades aparentemente ilimitadas de como as células T podem ser alteradas para combater uma doença específica. Contudo, numerosos exemplos de células T modificadas que causaram morbidade significativa e, em alguns casos, morte foram relatados. Assim, a toxicidade continua sendo a maior barreira para o uso generalizado de células T geneticamente modificadas. Ferramentas aprimoradas, como edição principal211 , a expressão controlada de moduladores imunológicos e interruptores de segurança permitirão, esperançosamente, terapias baseadas em células T de engenharia eficazes e seguras.
Ellis, GI, Sheppard, NC & Riley, JL Engenharia genética de células T para imunoterapia. Nat Rev Genet (2021). https://doi.org/10.1038/s41576-021-00329-9
- Aceitaram
- Publicados
- DOI https://doi.org/10.1038/s41576-021-00329-9