A abordagem rápida usada para combater o SARS-CoV-2 pode mudar o futuro da ciência das vacinas.
Quando os cientistas começaram a buscar uma vacina para o coronavírus SARS-CoV-2 no início de 2020, eles tiveram o cuidado de não prometer sucesso rápido. O mais rápido que qualquer vacina já havia sido desenvolvida, desde a amostragem viral até a aprovação, foi de quatro anos, para caxumba na década de 1960. Esperar por um até o verão de 2021 parecia altamente otimista.
Mas, no início de dezembro, os desenvolvedores de várias vacinas anunciaram excelentes resultados em grandes ensaios, com mais promissores. E em 2 de dezembro, uma vacina fabricada pela gigante farmacêutica Pfizer com a empresa de biotecnologia alemã BioNTech se tornou a primeira imunização totalmente testada a ser aprovada para uso de emergência .
Essa velocidade de avanço “desafia todo o nosso paradigma do que é possível no desenvolvimento de vacinas”, diz Natalie Dean, bioestatística da Universidade da Flórida em Gainesville. É tentador esperar que outras vacinas possam agora ser feitas em uma escala de tempo comparável. São extremamente necessários: doenças como malária, tuberculose e pneumonia juntas matam milhões de pessoas por ano , e os pesquisadores também prevêem mais pandemias letais.
A experiência do COVID-19 quase certamente mudará o futuro da ciência da vacina, diz Dan Barouch, diretor do Centro de Virologia e Pesquisa de Vacinas da Harvard Medical School em Boston, Massachusetts. “Isso mostra como o desenvolvimento de vacinas pode ser rápido quando há uma verdadeira emergência global e recursos suficientes”, diz ele. Novas formas de fazer vacinas, como o uso de RNA mensageiro (mRNA), foram validadas pela resposta do COVID-19, acrescenta. “Isso mostrou que o processo de desenvolvimento pode ser acelerado substancialmente sem comprometer a segurança.”
O mundo foi capaz de desenvolver vacinas COVID-19 tão rapidamente devido a anos de pesquisas anteriores sobre vírus relacionados e maneiras mais rápidas de fabricar vacinas, financiamento enorme que permitiu às empresas realizar vários testes em paralelo e reguladores agindo mais rapidamente do que o normal. Alguns desses fatores podem se traduzir em outros esforços de vacinas, especialmente plataformas de fabricação mais rápidas.
Mas não há garantia. Repetir esse sucesso rápido exigirá financiamento maciço semelhante para o desenvolvimento, o que provavelmente ocorrerá apenas se houver um senso comparável de urgência social e política. Dependerá, também, da natureza do patógeno. Com o SARS-CoV-2, um vírus que sofre mutação relativamente lenta e que pertence a uma família bem estudada, os cientistas podem – por mais estranho que pareça – ter sorte.
Anos de pesquisa avançada
A pesquisa que ajudou a desenvolver vacinas contra o novo coronavírus não começou em janeiro. Durante anos, os pesquisadores prestaram atenção aos coronavírus relacionados, que causam a SARS (síndrome respiratória aguda grave) e a MERS (síndrome respiratória do Oriente Médio), e alguns trabalharam em novos tipos de vacina – um esforço que agora tem valido a pena.
As vacinas convencionais contêm proteínas virais ou formas desativadas do próprio vírus, que estimulam as defesas imunológicas do corpo contra a infecção por um vírus vivo. Mas as duas primeiras vacinas COVID-19 para as quais a eficácia foi anunciada em ensaios clínicos de grande escala (fase III) usaram apenas uma cadeia de mRNA dentro de uma capa lipídica. O mRNA codifica uma proteína chave do SARS-CoV-2; assim que o mRNA entra em nossas células, nossos corpos produzem essa proteína. Ele atua como o antígeno – a molécula estranha que desencadeia uma resposta imunológica. As vacinas feitas pela Pfizer e BioNTech e pela empresa farmacêutica norte-americana Moderna utilizam mRNA que codifica a proteína spike, que se fixa nas membranas celulares humanas e permite que o coronavírus invada a célula.
“Muito foi investido na plataforma de mRNA que temos hoje”, diz a imunologista Akiko Iwasaki, da Yale School of Medicine em New Haven, Connecticut, que trabalhou em vacinas de ácido nucleico – aquelas baseadas em comprimentos de DNA ou RNA – para mais mais de duas décadas. A pesquisa básica sobre vacinas de DNA começou há pelo menos 25 anos, e as vacinas de RNA se beneficiaram de 10-15 anos de pesquisas intensas, diz ela, algumas voltadas para o desenvolvimento de vacinas contra o câncer . A abordagem amadureceu na hora certa; cinco anos atrás, a tecnologia de RNA não estaria pronta.
Por exemplo, pesquisadores do Instituto Nacional de Alergia e Doenças Infecciosas dos Estados Unidos (NIAID) em Bethesda, Maryland, sabiam, por meio de suas pesquisas sobre MERS e SARS, que era melhor ajustar a sequência de RNA para estabilizar a proteína spike resultante na forma que ela adota antes de acoplar a uma célula hospedeira. “Se você puder prendê-lo em seu estado original de pré-fusão, ele se tornará um antígeno de vacina muito melhor”, disse Barney Graham, vice-diretor do centro de pesquisa de vacinas do NIAID. Esse trabalho deu à equipe do NIAID, que trabalhou com a Moderna, uma vantagem depois que o SARS-CoV-2 foi sequenciado em janeiro. “O fato de que as pessoas estavam prestando muita atenção aos coronavírus realmente permitiu que todo o processo se acelerasse”, diz Dean.
A terceira vacina a mostrar eficácia em ensaios clínicos de fase III em novembro, feita pela empresa farmacêutica AstraZeneca com a Universidade de Oxford, no Reino Unido, não usa mRNA. Em vez disso, um vetor viral (ou portador) contém material genético extra que codifica para a proteína spike SARS-CoV-2. Isso também se beneficiou de anos de pesquisa para selecionar o vetor; neste caso, a empresa escolheu uma forma modificada de adenovírus isolado de fezes de chimpanzé. Avanços em vacinas convencionais como essas também vieram de pesquisas sobre SARS, MERS, Ebola e malária, diz Beate Kampmann, diretora do Centro de Vacinas da Escola de Higiene e Medicina Tropical de Londres, e tais abordagens permanecem mais baratas do que usar mRNA.
Os pesquisadores de vacinas tiveram sorte com o SARS-CoV-2 em muitos aspectos, diz Iwasaki. O vírus não sofre muitas mutações ou tem estratégias eficazes para frustrar o sistema imunológico humano, diz ela, ao contrário do HIV, do herpes ou mesmo da gripe. O vírus do herpes, por outro lado, tem mais capacidade de evasão – ele bloqueia ativamente a ligação de anticorpos, o que torna mais difícil encontrar um agente eficaz contra ele. E a rápida mutação dos vírus da gripe requer uma formulação de vacina diferente para cada temporada de gripe.
Supercharged com financiamento
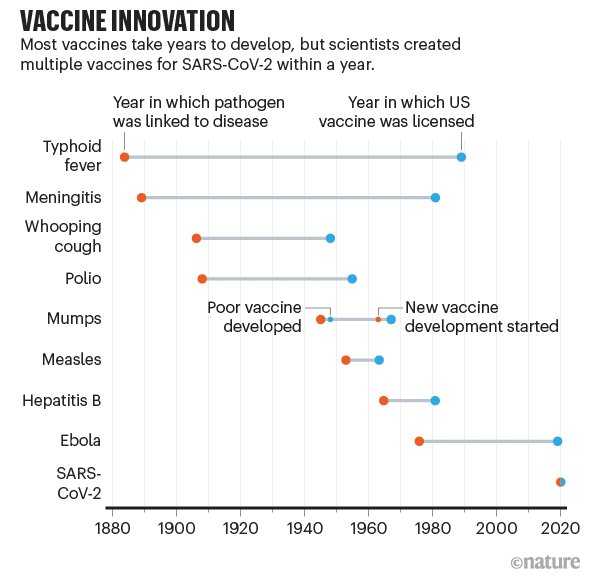
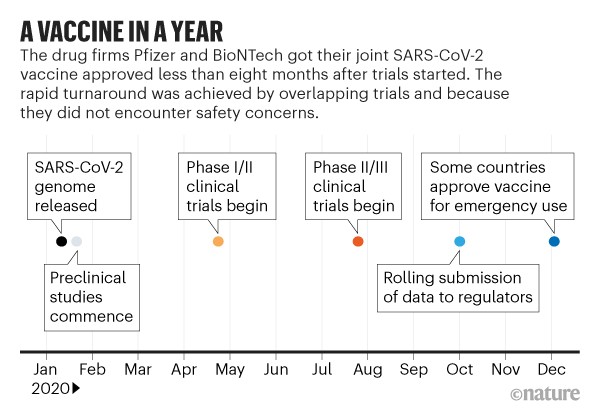
A parte mais lenta do desenvolvimento da vacina não é encontrar tratamentos candidatos, mas testá-los. Isso geralmente leva anos (consulte ‘Inovação em vacinas’), com empresas realizando testes de eficácia e segurança em animais e, em seguida, em humanos. O teste humano requer três fases que envolvem um número crescente de pessoas e custos proporcionalmente crescentes. As vacinas COVID-19 passaram pelos mesmos testes, mas os bilhões investidos no processo possibilitaram que as empresas corressem riscos financeiros realizando alguns testes ao mesmo tempo (consulte ‘Uma vacina em um ano’).
Fontes: Nosso mundo em dados; Análise da Nature
Com grandes somas dadas às empresas de vacinas por financiadores públicos e filantropos privados, “eles poderiam fazer testes pré-clínicos e de fase I, II e III, bem como fabricar, em paralelo em vez de sequencialmente”, diz Rino Rappuoli, cientista-chefe da divisão de vacinas da GlaxoSmithKline em Siena, Itália. Isso significava que as empresas podiam apostar no início de testes em grande escala e fabricação de candidatos que poderiam não funcionar. “Foi totalmente arriscado todo o processo de desenvolvimento”, diz Kampmann.
A ciência da vacina não teria produzido resultados tão rápidos sem este financiamento, diz ela. “Isso não aconteceu com o Ebola, que estava devastando comunidades na África [em 2014-16]” – e as vacinas contra o Ebola, consequentemente, demoraram mais para se desenvolver . O dinheiro só se materializou desta vez porque todos os países, inclusive os ricos, enfrentaram uma devastação econômica: sugerindo que o desenvolvimento de futuras vacinas, inclusive para doenças existentes como a malária, não será tão rápido. “A menos que você coloque o dinheiro, não há como acelerar”, diz Rappuoli.
O virologista Peter Hotez, do Baylor College of Medicine em Houston, Texas, sugere que as grandes empresas farmacêuticas podem ter sido motivadas não apenas pelo desejo de interromper a pandemia, mas também pela oportunidade de os governos financiarem sua pesquisa e desenvolvimento. Com investimento público de cerca de US $ 10 bilhões, o programa de vacinas da Operação Warp Speed dos EUA “representa o maior pacote de estímulo governamental que as empresas farmacêuticas já viram”, diz Hotez.
O ímpeto não veio totalmente da urgência da pandemia COVID-19 em si. Os vírus infecciosos e letais anteriores motivaram a criação de infraestruturas nacionais e globais que podem promover o desenvolvimento de vacinas mais rápido. Os surtos de Ebola e Zika deram início a uma melhor coordenação global em como responder a uma crise de doenças infecciosas, diz Graham. “Se a SARS em 2002 tivesse se espalhado assim, não teríamos a tecnologia de vacinas ou os sistemas coordenados e teríamos muito mais dificuldades”, diz ele.
Fontes: BioNTech / Pfizer; Análise da Nature
Em particular, a Coalition for Epidemic Preparedness Innovations (CEPI) foi lançada em 2017 ; seu objetivo é criar a infraestrutura tecnológica necessária para o desenvolvimento rápido e acessível de vacinas contra vários dos vírus conhecidos por ter potencial epidêmico, incluindo MERS, Ebola e Zika. O CEPI financiou parcialmente o trabalho com vacinas contra SARS-CoV-2, incluindo as da Moderna e Oxford.
Nos estágios finais dos testes, ajudou o fato de COVID-19 estar em toda parte porque as empresas precisam de infecções para mostrar que as vacinas funcionam. É difícil realizar testes de eficácia quando as próprias doenças não são prevalentes – especialmente, diz Dean, em casos como o MERS, para os quais os surtos da doença foram irregulares, com picos em algumas áreas e baixas taxas de infecção em outras.
A experiência COVID-19 também pode levar a um repensar regulamentar. Embora não tenha havido relaxamento dos critérios estritos para a aprovação da vacina, os primeiros candidatos estão, em sua maioria, sendo aprovados sob os regulamentos de uso de emergência. Estes são mais rápidos, mas exigem que as empresas conduzam pesquisas de acompanhamento para procurar efeitos colaterais e eficácia contínua. Os reguladores nacionais também trocaram informações sobre os ensaios de vacinas COVID-19 sob os auspícios de um organismo global chamado Coalizão Internacional de Autoridades Reguladoras de Medicamentos, criada em 2012. O objetivo é chegar a um consenso sobre questões como os melhores desfechos para ensaios de vacinas , e como harmonizar o monitoramento de efeitos colaterais conforme as vacinas são lançadas (ver também Nature 588, 195; 2020 ).
Benefícios para outras vacinas
A pandemia COVID-19 deve apresentar algumas mudanças permanentes no desenvolvimento da vacina. Para começar, pode estabelecer o uso de vacinas de mRNA – que não haviam sido previamente aprovadas para uso geral em pessoas – como uma abordagem rápida para outras doenças. “Essa tecnologia está revolucionando a vacinologia”, diz Kampmann. As vacinas de mRNA candidatas podem ser sintetizadas quimicamente em poucos dias , em contraste com a biotecnologia mais complicada envolvida na produção de proteínas nas células. “A tecnologia se presta à abordagem ágil plug-and-play que será necessária para responder a pandemias [futuras]”, diz Kampmann.
Além do mais, “o RNA simplifica muito a fabricação”, diz Rappuoli. “Você pode usar a mesma facilidade para fazer RNA para doenças diferentes. Isso diminui o investimento necessário. ” As empresas também devem aumentar suas capacidades de fabricação porque ainda precisam fazer vacinas contra sarampo, poliomielite e outras doenças, mesmo quando produzem imunizações COVID-19. Isso pode ajudar a atender a demanda no futuro.
A vacina de mRNA COVID-19 da Moderna será produzida pela empresa de biotecnologia Lonza nessas instalações em Visp, Suíça. Crédito: Denis Balibouse / Reuters
Os grandes ensaios clínicos para vacinas COVID-19, e outras em desenvolvimento, devem fornecer dados que são mais amplamente úteis para a compreensão das respostas imunológicas, diz Hotez. “Dadas todas as diferentes tecnologias e informações detalhadas coletadas sobre dados demográficos clínicos voluntários, anticorpos e respostas celulares, podemos aprender tanto ou mais com as respostas às vacinas humanas este ano do que nas décadas anteriores. A vacinologia humana pode dar um salto quântico. ”
Ainda assim, outras vacinas provavelmente só podem ser desenvolvidas em uma velocidade comparável quando os níveis de infecção são altos – tornando possível realizar testes massivos com relativa rapidez – e com enormes quantias de financiamento. E outros vírus podem ser mais difíceis de atacar do que o SARS-CoV-2 acabou sendo.
É por isso que precisamos saber mais sobre todas as famílias de vírus, dizem os pesquisadores. Existem pelo menos 24 outras famílias de vírus que podem infectar humanos, diz Graham. Em vez de esperar para gastar recursos na luta contra o próximo vírus que surgir, o dinheiro seria melhor gasto agora configurando sistemas para monitorar todos esses vírus e gerar dados sobre infecções de protótipo em cada uma dessas famílias, diz ele.
Em outras palavras, nenhuma quantia de dinheiro ajudará sem uma plataforma sólida de ciência básica para construir. O extraordinário sucesso das vacinas COVID-19 “é um bom exemplo do que a ciência pode fazer muito rapidamente”, diz Iwasaki, “mas não aconteceu da noite para o dia”.