Michele Ramos da Silva
Orientador(a): Prof. Dra.Franciele Cascaes
Co-orientador(a): Prof. Msc. Natália Quintanilha
Universidade do Sul de Santa Catarina – UNISUL
Resumo
O ano de 2020, assim como ocorre em 2021, foi marcado pela pandemia da COVID-19, doença que é causada pelo vírus SARS-CoV-2. Os primeiros casos da doença foram registrados na China no final de 2019, e no dia 11 de março de 2020 a Organização Mundial da Saúde (OMS) decretou estado de pandemia devido à rápida expansão da doença por diversos lugares do mundo. O cenário de incertezas com a falta de tratamentos e fármacos específicos, promoveu uma corrida científica para identificar processos biológicos que envolvem o vírus e a célula hospedeira. Genomas virais são capazes de codificar todas as proteínas que necessitam para sua expansão, eles controlam toda a maquinaria celular do hospedeiro visando o domínio na regulação da proliferação celular, apoptose e imunidade. Identificar os processos da infecção viral provocada por SARS-CoV-2 desde a transcrição de seu material genético, da síntese de proteínas e da regulação da expressão gênica, pode auxiliar na descoberta de potenciais alvos terapêuticos para utilização em terapias mais efetivas no combate à COVID-19. Um mecanismo muito importante, descoberto a pouco mais de 20 anos vem se destacando sobre sua ação no controle da expressão gênica, trata-se da ação dos microRNAs (miRNAs), que podem atuar na ativação ou inativação RNA mensageiros (mRNA). O objetivo do estudo foi analisar a produção científica sobre as possíveis variações na expressão de miRNAs após infecção por SARS-CoV-2, através da previsão de alvos de miRNAs no genoma viral, auxiliando na compreensão de processos e assim colaborar com a terapêutica para a doença.
Palavras chave: SARS-CoV, SARS-CoV-2, RNA, miRNA, COVID- 19.
Abstract
The year 2020, as in 2021, was marked by the pandemic of COVID-19, a disease that is caused by the SARS-CoV-2 virus. The first cases of the disease were recorded in China in late 2019 and on March 11, 2020, the World Health Organization (WHO) decreed a state of pandemic due to the rapid expansion of the disease in different parts of the world. The scenario of uncertainties with the lack of specific treatments and drugs, promoted a scientific race to identify biological processes that involve the virus and the host cell. Viral genomes are to encode all the proteins they describe for their expansion, they control all the host’s cellular machinery, the domain in the regulation of cell proliferation, apoptosis and immunity. Identifying the processes of viral infection caused by SARS-CoV-2 since the transcription of its genetic material, the synthesis of proteins and the regulation of gene expression, can assist in the discovery of potential therapeutic targets for use in more effective therapies to combat COVID-19 . A very important mechanism, discovered a little more than 20 years ago, has stood out over its action in the control of gene expression, it is the action of micro RNAs (miRNAs), which can act in the activation or inactivation of messenger RNA (mRNA). The objective of this work was analyzed as the possible variations in the expression of miRNAs after infection by SARS-CoV-2, through the prediction of targets of miRNAs in the viral genome, helping to understand processes and thus collaborate with therapy for the disease.
Key words: SARS-CoV, SARS-CoV-2, RNA, miRNA, COVID- 19.
Introdução
COVID-19 é o nome dado à Síndrome Respiratória Aguda Grave Coronavírus 2, provocada pelo novo vírus, da família dos Coronavírus, denominado de SARS-CoV-2. A doença teve suas primeiras manifestações no final de 2019, em Wuhan, na China. Sua expansão foi muito expressiva e em poucos meses levou ao cenário de pandemia. Este novo vírus, é o sétimo coronavírus que pode infectar seres humanos, ele está entre os mais graves junto ao MERS-CoV (Síndrome Respiratória do Oriente Médio – 2012) e SARS-CoV (Síndrome Respiratória Aguda Grave – 2002), que provocaram surtos nos últimos anos (ISER et al., 2020).
Todo o genoma do SARS-CoV-2 contém menos de 30.000 nucleotídeos, aproximadamente 29 diferentes proteínas sintetizadas pelo vírus já foram identificadas; entre elas, as mais relevantes são a (S) Spike e (N) do nucleocapsídeo viral. A glicoproteína de pico (S) permite a entrada do vírus na célula hospedeira e a proteína do nucleocapsídeo, por sua vez, regula o processo de replicação viral (UZUNIAN, 2020).
O principal papel dos vírus ao infectar uma célula é reproduzir suas próprias proteínas, duplicar seu genoma e reconstruir suas estruturas, assim, formam complexos com mRNAs ou proteínas no hospedeiro para iniciar a regulação da expressão gênica, promovendo a inibição ou a tradução de sistemas regulatórios para auto favorecimento. Neste contexto, um pequeno RNA não codificante (ncRNA), chamado de microRNA (miRNA), que tem como função atuar na regulação da expressão gênica, vem sendo estudado. Os miRNAs do hospedeiro podem atuar de diversas formas, uma delas é impedindo a entrada do vírus na célula, atuando através da degradação do mRNA responsável pela expressão da enzima conversora da angiotensina 2 (ACE2), que é a responsável pela ancoragem do vírus na membrana celular hospedeira (PIERCE, et al., 2020).
Os miRNAs são classificados como pequenos RNAs endógenos não codificadores do código genético, em nível pós transcricional e seu tamanho varia aproximadamente de 21 a 23 nucleotídeos; eles são complementares a determinadas regiões do mRNA, promovendo tanto o bloqueio do processo de tradução quanto a degradação destes alvos (BARTEL, 2009). A especificidade dos alvos de miRNAS acontecem entre suas sequências chamadas de semente, nas posições 2 a 8 da sua extremidade 5’, e a sequência que corresponde a semente no mRNA, é na sua extremidade 3’ não traduzida (LUJAMBIO; LOWE, 2012).
Diante disso, o objetivo do estudo foi analisar a produção científica sobre as possíveis variações na expressão de miRNAs após infecção por SARS-CoV-2, através da previsão de alvos de miRNAs no genoma viral, auxiliando na compreensão de processos e assim colaborar com a terapêutica para a doença.
Métodos
Trata-se de uma revisão narrativa baseada em artigos científicos publicados em revistas digitais da área da ciência e saúde. No que tange ao levantamento bibliográfico foram consultadas a Biblioteca Virtual em Saúde (BVS), Medical Literature Analysis and Retrieval System Online (MEDLINE) via PUBMED e Scientific Electronic Library Online (SciELO) com os seguintes critérios de inclusão: estudo com a temática miRNAs viral e hospedeiro e seus possíveis alvos envolvidos em processos imunológicos e de infestação viral, além de variações destes durante infecção. Foram excluídos os artigos de revisão, que não apresentaram dados significativos sobre a identificação e variação de miRNAs durante a infecção por SARS-CoV-2. Foram utilizados os seguintes descritores controlados: SARS-CoV, SARS-CoV-2, RNA, miRNA, COVID- 19.
A coleta de dados foi realizada durante o mês de outubro de 2020 até março de 2021. A análise dos artigos ocorreu de forma descritiva e os resultados foram apresentados em forma de quadros, possibilitando ao leitor da revisão avaliar as características de cada artigo.
Resultados
A busca nas bases de dados identificou 20 artigos. Após a leitura dos artigos na íntegra, foram excluídos 15 estudos por não contemplarem os critérios de inclusão, restando cinco artigos incluídos nesta revisão. A Figura 1 demonstra o fluxograma dos estudos incluídos e o quadro 1 apresenta a descrição dos estudos incluídos, segundo nome da revista, autores, ano de publicação, título do estudo, metodologia de análise do miRNA e miRNA de interesse.
Figura 1. Diagrama do resultado da aplicação dos critérios de inclusão e exclusão de artigos para o estudo. Florianópolis, SC. 2021.
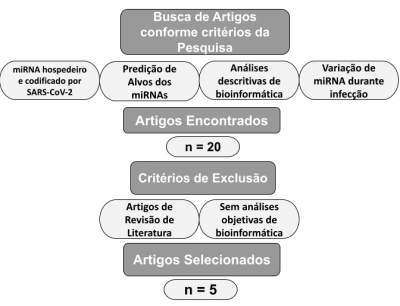
Fonte: Elaborado pela autora, 2021.
Diante das análises dos artigos selecionados, foi criado um quadro comparativo para elucidar as principais informações, observou-se o uso de diversas ferramentas de bioinformática, através das quais foi possível chegar a diversos resultados.
Quadro 1. Características dos estudos incluídos
| Autores/Ano | Revista | Título | Metodologia |
| CHOW, 2020. | Genes | Predição e análise de segmentação SARS-CoV-2 MicroRNA em epitélio pulmonar humano | TargetScan: predição de alvo de miRNA, RNA22: predição de alvo e cálculo de energia livre, TCGA-LUAD: dados de expressão de miRNA seq. em tecido normal, Genbank: análise genoma viral, NCBI geo: sequenciamento de miRNA, edgeR: cálculo da expressão diferencial em SARS-CoV-2 em comparação com células infectadas |
| LIU, 2020. | Cornell University | Implicações do miRNA codificado por vírus e miRNA do hospedeiro na patogenicidade de SARS-CoV-2 | NCBI: genoma de SARS-CoV-2, VMir v2.2,HuntMi e Maturebayes: MiRNAs, Enhancer Atlas, TargetScan, TargetFinder e MiRanda e TargetScanHuman 7.2, Gene Ontology, GOstats; Previsão de alvos |
| LI, 2020. | Journal Of Clinical Laboratory Analysis | Expressão diferencial de microRNA no sangue periférico de pacientes humanos com COVID-19 | Prática: Extração, Purificação, PCR. miRdeep2: genoma viral. miRanda: previsão de alvos. Gene Ontology : análise de expressão diferencial. |
| ALAM, 2020. | Mdpi: Non-Coding RNA | miRCOVID-19: Alvos potenciais de miRNAs humanos em SARS-CoV-2 para descoberta de drogas baseadas em RNA | MiRBase: miRNAs maduros, RNA22: miRNA humano, GenBank: genoma HCV, NCBI: genoma SARS-CoV-2, miRtap e miRanda: alvos de miRNA no genoma de SARS-CoV-2, FANTOM: expressão de miRNAs que se ligam ao vírus da COVID19, BEDTools: sobreposição de locais previstos e regiões estruturadas conservadas e não estruturadas conservadas no SARS-CoV-2, Gene Ontology: possíveis vias de atuação dos miRNAs e Enciclopédia de Genes e Genomas de Kyoto (KEGG) |
| ARISAN, 2020. | Viruses | A previsão de miRNAs em genomas SARS-CoV-2: bancos de dados hsa-miR identificam 7 miRs-chave vinculados a respostas do hospedeiro e vias KEGG relacionadas à patogenicidade do vírus significativas para comorbidades | NCBI: genoma SARS-CoV-2 de China, Itália, Espanha e MERS, SARS, OC43 e 229E. GISAID: genoma SARS-CoV-2 da Inglaterra e Turquia. miRTarget e miRBase: prever as semelhanças entre o genoma SARS-CoV-2 e miRNAs humanos. NCBI BioProject: biópsias de pulmão de pacientes infectados com SARS-CoV-2 e voluntários saudáveis. topGO R: enriquecimento de vias, ontologia genética, estrutura de domínio e outras ontologias |
Fonte: Elaborado pela autora, 2021.
Chow e Salmena (2020) basearam sua pesquisa na hipótese que miRNAs podem mediar mecanismos de defesa intracelular contra vírus de RNA e que a alta expressão de miRNAs específicos pode ser um efetivo mecanismo de defesa em tecido epitelial pulmonar, como também a baixa expressão pode ser um mecanismo que auxilie na suscetibilidade à infecção. Assim, buscaram identificar miRNAs com sítios de ligação no genoma do SARS-CoV-2, iniciaram a pesquisa fazendo predição de alvos de miRNAs no genoma viral, realizaram cálculos de energia de ligação para terem fortes candidatos, observaram a expressão de genes em tecidos normais e encontraram 128 candidatos com potencial a atingir o genoma viral, destes, 46 são expressos em tecido sem infecção. Após a infecção, foram feitas análises de expressão diferencial (DEA) e os resultados comprovaram que ocorreram alterações nos padrões de expressão de 45 miRNAs, com 17 miRNAs regulados de forma positiva e 28 de forma negativa. Depois foi realizado um cruzamento de dados entre os 128 candidatos a alvos e os 45 miRNAs diferencialmente expressos; e apenas 6 miRNAs estavam relacionados, quatro tipos com baixa regulação (hsa-let-7a-3p, hsa-miR-135b-5p, hsa-miR-16-2-3p e hsa-miR 1275) e dois com alta regulação (hsa-miR-155-3p e hsa-miR-139-5p). Por fim, entre esses seis apenas dois foram diferentemente expressos no tecido epitelial pulmonar, o hsa-let-7a-3p e o hsa-miR-155-3p, objetivo do estudo.
O estudo de Liu et al. (2020), analisou quais as implicações do miRNA viral e hospedeiro na patogenicidade da infecção por SARS-CoV-2. Os autores identificaram o genoma viral no banco de dados National Center for Biotechnology Information (NCBI), pré-miRNAs virais com VMir Analyzer e MatureBayes resultando em 90 miRNAs codificadas pelo vírus. Esses miRNAs virais podem assumir tanto o papel de suprimir como o de ativar a expressão de genes do hospedeiro durante a infecção; como exemplo de repressão o md2-5p e mR 147-3p virais interagem com genes responsáveis pela síntese de proteínas pró apoptóticas, pela verificação do ciclo celular, processos de síntese de fatores de transcrição, regulação da gliconeogênese, regulação da glicose e lipídios e cascata de sinalização para suprir necessidades virais. Outros miRNAs virais que atuam nos principais tecidos atingidos pela doença foram identificados, miRNA viral MR 147-5p possui como alvos os genes no tecido pulmonar que atuam no aumento da inflamação e organização do citoesqueleto celular, que ao serem super expressos favorecem a invasão do SARS-CoV-2 na célula hospedeira. No intestino MR 147-3p é o miRNA que age sobre o TMPRSS2, que codifica a serina protease transmembranar (TMPRSS2) como também a enzima conversora de angiotensina 2 (ECA2), importantes aliadas na ancoragem e entrada do vírus na célula. No fígado o miRNA sintetizado pelo vírus, MR 198-3p potencializa o gene responsável pela adenosina desaminase, que suprime respostas do sistema interferon em infecções por vírus, demonstrando como os miRNAs virais podem controlar sistemas do hospedeiro para realizar seus processos de replicação, remontagem e infestação. Outro tecido que analisaram foi o baço onde foi previsto que o MR 66-3p age intensificando a liberação de Fator de Necrose Tumoral (TNF-α) que participa da tempestade de citocinas. Encontraram indícios da atuação de mais miRNAs virais como, MR 359-5p e MR 328-5p, sobre todos os tecidos analisados, estes agem em genes que fortalecem a fixação do vírus a seus receptores, e atenuam a resposta do hospedeiro ao suprimir a síntese de Interferon tipo I. Além da atuação de miRNAs virais, o estudo levantou a possibilidade do vírus sequestrar e mudar a função dos miRNAs do hospedeiro, essa hipótese se deu pela atuação similar com outras infecções, sugerindo por exemplo que o miR-27, miR-146 e miR-939 podem modular cerca de 800 genes humanos, e seu sequestro interfere diretamente na atividade anormal da imunidade. Em paralelo aos miRNAs virais foram encontrados 28 miRNAs do hospedeiro com alvos previstos em 30 genes do vírus, todas regiões que produzem enzimas para replicação viral e tradução. Destaque para o hsa-miR-4661-3p que foi previsto para atuar no gene S, de forma a reprimir a expressão da proteína S viral, dando um bom exemplo de um mecanismo antiviral.
Com uma abordagem mais prática, no estudo de LI et al. (2020), os autores analisaram amostras de 10 pacientes infectados pela COVID19 e quatro doadores saudáveis. Após ser extraído e purificado o RNA foi sequenciado, e com análises de bioinformática foi feita correlação dos miRNAs com seus possíveis genes alvos. Na comparação dos pacientes infectados com os saudáveis, as amostras com COVID resultaram em 35 miRNAs regulados positivamente e 38 negativamente. Destes, destaque para o hsa-miR-16-2-3P que foi o mais regulado, enquanto hsa-miR-6501-5P teve o maior aumento de expressão, e hsa-miR-627-5p e hsa-miR-183-5p com a menor regulação.
No artigo de Alam e Lipovich (2021), os autores buscaram comparar o genoma do vírus da hepatite C (HCV) e seus sítios de ligação de miRNAs com o genoma de SARS-CoV-2. Um exemplo foi o miR-122 que na HCV age estabilizando o genoma viral para facilitar sua infestação, então o desenvolvimento de Anti-miRs ou antagomiRs; que são drogas de oligonucleotídeos com estrutura química modificada para inativar miRNAs; podem impedir a hibridização de miR-122 com genoma viral bloqueando a replicação viral. Com as análises, os autores desenvolveram uma plataforma de meta análise computacional, o miRCOVID-19, que destaca alvos de miRNAs humanos no genoma de SARS-CoV-2. Após essa análise observaram que estes alvos podem estar em diversas regiões, incluindo nos genes que codificam proteínas estruturais virais, com as proteínas M,N e S, como também nos genes que codificam proteínas não estruturais (Nsps), ainda identificaram outras regiões como a estruturada conservada, com alvos para os miRNAs hsa-miR-122-5p, hsa-miR-1304-5p, hsa-miR-885-3p, hsa-miR-598-5p, hsa-miR-6834-5p, hsa-miR-514b-5p, hsa-miR-1910-5p, hsa-miR-766-3p, hsa-miR-1912 -5p, hsa-miR-187-5p, e a região não estruturada conservada de SARS-CoV-2 com alvos dos miRNAs hsa-miR-296-3p e hsa-miR-1304-5p.
De acordo com ARISAN, Elif Damla et al.(2020) após comparações do SARS-CoV-2 com MERS, SARS e dois resfriados comuns, OC43 e 229E, relataram que a maior relação de conservação das características genômicas foi entre o genoma de SARS e SARS-CoV-2, com destaque para o hsa-miR-1468 que foi completamente conservado. Também foi abordado no estudo cinco sequências do genoma de SARS-CoV-2 de diferentes regiões: China, Itália, Espanha, Inglaterra e Turquia, com o objetivo de encontrar semelhanças entre alvos de miRNAs hospedeiros. Trouxeram como resultado sete miRNAS o hsa-miR-8066, hsa-miR-5197, hsa-miR-3611, hsa-miR-3934-3p, hsa-miR-1307-3p, hsa-miR-3691-3p e hsa-miR 1468-5p, e a abordagem conhecida de cada um deles. Uma grande contribuição deste artigo foi a análise de vias de atuação com base na Enciclopédia de Kyoto de Genes e Genomas (KEGG), dados que podem auxiliar na relação da infectividade da doença com comorbidades.
Todos os estudos apresentaram contribuições significativas e destacaram um ou mais miRNAs importantes conforme Quadro 2.
Quadro 2. Quadro comparativo dos miRNAs evidenciados nos estudos.
| Artigos | miRNAs | miRNA Destaque |
| Predição e análise de segmentação SARS-CoV-2 MicroRNA em epitélio pulmonar humano | baixa regulação (hsa-let-7a-3p, hsa-miR-135b-5p, hsa-miR-16-2-3p e hsa-miR 1275), e alta regulação (hsa-miR-155- 3p e hsa-miR-139-5p) | a)Baixa regulação hsa-let-7a-3p e alta regulação hsa-miR-155- 3p. |
| Implicações do miRNA codificado por vírus e miRNA do hospedeiro no patogenicidade de SARS-CoV-2 | miRNA Viral: md2-5p, mR 147-3p, MR 147-5p, MR 147-3p, MR 198-3p, MR 66-3p, MR 359-5p e MR 328-5p. miRNA hospedeiro: hsa-miR-27, hsa-miR-146, hsa-miR-939, hsa-miR-4661-3p | b) hsa-miR-4661-3p. |
| Expressão diferencial de microRNA no sangue periférico de pacientes humanos com COVID-19 | hsa-miR-16-2-3P, hsa-miR-5695, hsa-miR-10399-3P, hsa-miR-6501-5P, hsa-miR-361-3P, hsa- miR ‐ 361‐3p, hsa ‐ miR ‐ 4659a ‐ 3p, hsa ‐ miR ‐ 142‐5p, hsa ‐ miR ‐ 4685‐3p, hsa ‐ miR ‐ 454‐5p e hsa ‐ miR ‐ 30c ‐ 5p. hsa-miR-183-5p, hsa-miR-627-5p, hsa-miR-941, hsa-miR-21-5p, hsa-miR-20a-5p, hsa ‐MiR ‐ 146b ‐ 5p, hsa ‐ miR ‐ 454‐3p, hsa ‐ miR ‐ 18a ‐ 5p, hsa ‐ miR ‐ 340‐5p e hsa ‐ miR ‐ 17‐5p. | c) Mais regulado hsa-miR-16-2-3P, maior expressão hsa-miR-6501-5P. |
| miRCOVID-19: Alvos potenciais de miRNAs humanos em SARS-CoV-2 para descoberta de drogas baseadas em RNA | hsa-miR-122-3p, hsa-miR-1307-3p, hsa-miR-766-3p, hsa-miR-1910-5p, hsa-mir-296-3p, hsa-miR-1304-5p, hsa-miR-187-5p, hsa-miR-885-3p, hsa-miR-1912-5p, hsa-miR-4761-5p, hsa-miR-598-5p, hsa-miR-6834-5p, hsa-miR-514b-5p e hsa-miR-149-3p | d) hsa-miR-122-3p. |
| A previsão de miRNAs em genomas SARS-CoV-2: bancos de dados hsa-miR identificam 7 miRs-chave vinculados a respostas do hospedeiro e vias KEGG relacionadas à patogenicidade do vírus significativas para comorbidades | hsa-miR-8066, hsa-miR-5197, hsa-miR-3611, hsa-miR-3934-3p, hsa-miR-1307-3p, hsa-miR-3691-3p, hsa-miR 1468-5p | e) hsa-miR-8066. |
Fonte: Elaborado pela autora, 2021.
Discussão
Os trabalhos selecionados apresentaram dados sobre a variação da expressão de alguns miRNAs, que correspondem à maneira como o vírus SARS-Cov-2 age no hospedeiro, tanto ativando a expressão de genes quanto suprimindo. De forma geral, a maioria dos miRNAs encontrados demonstram papel importante na subversão da defesa da célula infectada. Além disso, foi possível observar que os miRNAs ajudam na proliferação viral, que podem burlar o sistema imune do hospedeiro como também a supressão daqueles que possuem como alvos o gene viral, sugerindo assim estudos mais aprofundados para possíveis alvos terapêuticos.
O estudo de Chow e Salmena (2020), trouxe destaque para o miRNA hsa-let-7a-3p que teve sua regulação negativa durante a doença COVID-19. Este miRNA é um supressor tumoral, e sua regulação negativa pode refletir na desregulação da apoptose, impossibilitando de a célula induzir sua morte programada como forma de conter a invasão viral. Muitos estudos indicam que sua ação relaciona-se com os processos de divisão, diferenciação e proliferação celular, este miRNA também é muito relatado em associação ao câncer de pulmão (MASOOD; YASMIN, 2017). Já o miRNA apontado com regulação positiva, o hsa-miR-155-3p, também é um miRNA oncogênico, quando se encontra superexpresso, atuando em genes supressores de tumor como também na síntese de proteínas como interleucina-2 e interferon γ, que são reguladores pró inflamatórios que participam ativamente da tempestade de citocinas, característica da infecção pelo SARS-CoV-2 (SOLTANI et al., 2021). Sobre a tempestade de citocinas ou Síndrome de liberação de citocinas (SRC), que é uma resposta imunológica excessiva, foi analisado por Li et al.(2020), que os processos biológicos mais enriquecidos na infecção são as sínteses protéicas que levam ao quadro da síndrome. Seus estudos também apresentaram o hsa-miR-16-2-3P como o miRNA mais regulado, ele é um gene anti-apoptótico envolvido na morte celular programada, suas elevações podem induzir paradas no ciclo celular (HAN et al., 2019), e tem como alvo o fator de crescimento endotelial vascular (VEGF), sua repressão acarreta em problemas angiogênicos, enquanto o hsa-miR-6501-5P teve o maior aumento de expressão, ele age no complexo de lipídio quinase PI4KA, que participa das modificações das membranas celular e da mitocôndria, favorecendo a replicação viral e montagem do vírion. Ainda sobre a SRC o miRNA hsa-miR-8066 mostrou que sua expressão é diretamente relacionado a genes reguladores de citocinas, como também a processos de sepse na infecção por SARS-CoV-2, como trouxeram ARISAN et al.(2020).
A conexão entre os artigos revelou que os miRNAs virais possuem alvos nos genes da célula hospedeira para regulação de processos de controle apoptótico, imunidade e proliferação celular, além de atuar no próprio gene viral, com síntese de proteínas necessárias a seu desenvolvimento. Como exemplos dos miRNAs virais, o MD2-5p modula o gene CHAC1 (sintetiza uma enzima pró – apoptótica ), MR147-3p que atua sobre RAD9A (proteína de ponto de verificação do ciclo celular, que regula a morte celular e promove a apoptose), também MR359-5p sobre o gene FOXO3 (necessário para respostas antioxidantes e autofagia), MR385-3p foi previsto para se ligar a 5′-UTR de TGFBR3 , um gene amplamente expresso em células do sistema imune inato e adaptativo. MD2-5p foi direcionado para ENOX1, que codifica uma proteína que se apresenta no compartimento de citoesqueleto de células endoteliais (LIU et al. 2021). Neste aspecto fica clara a manobra de burlar o sistema de defesa celular. Também importante destacar ação de miRNAs contra o genoma viral, e o hsa-miR-4661-3p foi um exemplo de que sua regulação positiva poderia ser um ataque terapêutico, pois sua ação é associada à proteína S, sua ligação à extremidade 3’ UTR do gene viral S impede a síntese da proteína que forma a estrutura do vírus, como sugerido por Liu et al.(2020). Devido ao fato de ser um vírus novo, muitos estudos buscaram relacionar mecanismos de atuação viral com outros vírus conhecidos, como o da hepatite C (HCV), que apresenta similaridade entre seu genoma e seus sítios de ligação de miRNAs humanos, mesmos sítios previstos para o genoma de SARS-CoV-2. O miR-122 é um exemplo dos miRNAs relatados por Alam e Lipovich (2021), com base em estudos do genoma de HCV, ele tem ligação direta à 5 ‘UTR do genoma viral e sua ação está associada ao aumento no metabolismo lipídico e de colesterol durante a infecção, mecanismo utilizado pelo vírus para aumentar a inflamação.
Apesar do volume crescente de estudos sobre interações de miRNAs virais e hospedeiro durante infecção pelo SARS-CoV-2, ainda há necessidade de muitos estudos em relação a estes pequenos RNAs, devido suas inúmeras interações um único miRNA pode combinar com diversos mRNAs, o que deve ser extremamente conhecido e detalhado para que possam ocorrer interações terapêuticas sem efeitos adversos. Outro aspecto relevante é o avanço da bioinformática que auxilia as pesquisas, são diversas ferramentas e bancos de dados que permitem consultas e previsão de resultados que seriam praticamente impossíveis se fossem de forma manual.
Conclusão
A análise da produção científica no período de outubro de 2020 até maio de 2021 permitiu concluir que ainda são poucas as evidências do mecanismo de ação dos miRNAs, assim não houve nenhuma resposta exata sobre como são regulados os processos fisiológicos e como são afetados pelo vírus SARS-CoV-2. Entretanto, foi possível ver a contribuição da bioinformática nas previsões de alvos de miRNA viral e do hospedeiro. Mesmo com muito a ser estudado foi possível relacionar miRNAs já conhecidos, como o hsa-let-7a-3p, hsa-miR-155-3p, hsa-miR-4661-3p, hsa-miR-16-2-3P, hsa-miR-6501-5P, miR-122, hsa-miR-8066, em outras infecções ou patologias como do câncer, envolvidos em processos imunológicos e com isso mensurar nos tecidos mais atingidos, sobre variações em suas expressões o que demonstra um potencial caminho terapêutico contra a infecção por COVID-19 e suas consequências patológicas.
Referências
ALAM, Tanvir; LIPOVICH, Leonard. MiRCOVID-19: Potential Targets of Human miRNAs in SARS-CoV-2 for RNA-Based Drug Discovery. Mdpi: Non-Coding RNA, [s. l], v. 1, n. 7, p. 1-18, 02 mar. 2021. Trimestral. Disponível em: https://www.mdpi.com/2311-553X/7/1/18/htm. Acesso em: 20 abr. 2021.
AMERES, Stefan L.; ZAMORE, Phillip D.. Diversifying microRNA sequence and function. Nature: Nature Reviews Molecular Cell Biology, [S.L.], v. 14, n. 1, p. 475-488, 26 jun. 2013. Disponível em: https://www.nature.com/articles/nrm3611. Acesso em: 23 nov. 2020.
ARISAN, Elif Damla et al. The Prediction of miRNAs in SARS-CoV-2 Genomes: hsa-mir databases identify 7 key mirs linked to host responses and virus pathogenicity-related kegg pathways significant for comorbidities. Viruses, [S.L.], v. 12, n. 6, p. 614-620, 4 jun. 2020. MDPI AG. http://dx.doi.org/10.3390/v12060614. Disponível em: https://www.mdpi.com/1999-4915/12/6/614/htm. Acesso em: 20 abr. 2021.
BARTEL, David P. MicroRNAs: target recognition and regulatory functions. Cell: Science that inspires, [S.L.], v. 136, n. 2, p. 215-233, 23 jan. 2009. Disponível em: https://pubmed.ncbi.nlm.nih.gov/19167326/. Acesso em: 23 nov. 2020.
BORGES, Dayane (ed.). DNA e RNA – Definição, características, principais diferenças e funções. 2020. Disponível em: https://conhecimentocientifico.r7.com/dna-e-rna/. Acesso em: 24 dez. 2020.
BRASIL. Ministério da Saúde. Ministério da Saúde (ed.). Ministério da Saúde: coronavírus (covid-19). Coronavírus (COVID-19). 2020. Disponível em: https://coronavirus.saude.gov.br/sobre-a-doenca. Acesso em: 26 nov. 2020.
BRASIL. Organização Pan Americana da Saúde. Opas. OPAS/OMS Brasil: OMS afirma que COVID-19 é agora caracterizada como pandemia. 2020. Disponível em: https://www.paho.org/bra/index.php?ption=com_content&view=article&id=6120:oms-afirma-que-covid-19-e-agora-caracterizada-como-pandemia&Itemid=812. Acesso em: 26 nov. 2020.
CHOW, Jonathan Tak-Sum; SALMENA, Leonardo. Prediction and Analysis of SARS-CoV-2-Targeting MicroRNA in Human Lung Epithelium. Genes, [S.L.], v. 11, n. 9, p. 1002, 26 ago. 2020. MDPI AG. http://dx.doi.org/10.3390/genes11091002. Disponível em: https://www.mdpi.com/2073-4425/11/9/1002. Acesso em: 19 abr. 2021.
COX, Michael M.; et al. Biologia Molecular: princípios e técnicas. Porto Alegre: Artmed, 2012.
FABIAN, Marc Robert; SONENBERG, Nahum; FILIPOWICZ, Witold. Regulation of mRNA Translation and Stability by microRNAs. Annual Review Of Biochemistry, [S.L.], v. 79, n. 1, p. 351-379, 7 jun. 2010. Annual Reviews. http://dx.doi.org/10.1146/annurev-biochem-060308-103103. Disponível em: https://www.annualreviews.org/doi/pdf/10.1146/annurev-biochem-060308-103103. Acesso em: 23 nov. 2020.
HAFNER, Markus et al. Transcriptome-wide identification of RNA-binding protein and microRNA target sites by PAR-CLIP. Cell: Science that inspires, [S.L.], v. 1, n. 141, p. 129-141, 02 abr. 2010. Disponível em: https://www.cell.com/fulltext/S0092-8674(10)00245-X. Acesso em: 23 nov. 2020.
HAN, Tao et al. MiR-16-2-3p inhibits cell proliferation and migration and induces apoptosis by targeting PDPK1 in maxillary primordium mesenchymal cells. International Journal Of Molecular Medicine, [S.I.], v. 3, n. 43, p. 1441-1451, 21 jan. 2019.
ISER, Betine Pinto Moehlecke et al. Definição de caso suspeito da COVID-19: uma revisão narrativa dos sinais e sintomas mais frequentes entre os casos confirmados. Epidemiologia e Serviços de Saúde, Brasília, v. 29, n. 3, e2020233, jun. 2020. FapUNIFESP (SciELO). http://dx.doi.org/10.5123/s1679-49742020000300018. Disponível em: https://www.scielo.br/scielo.php?pid=S2237-96222020000300401 & script= sci_abstract & tlng=pt. Acesso em: 23 dez. 2020.
JORDÃO, Berenice Quinzani; ANDRADE, Celia Guadalupe T. J. (org.). Ciclo Celular e Meiose: a replicação do dna é semiconservativa. In: JUNQUEIRA, Luiz Carlos Uchoa; CARNEIRO, José. Biologia Molecular e Celular. 9. ed. Rio de Janeiro: Guanabara Koogan, 2012. Cap. 9. p. 181-187.
KIM, Dongwan et al. The Architecture of SARS-CoV-2 Transcriptome. Cell, [S.L.], v. 181, n. 4, p. 914-921, 14 maio 2020. Disponível em: https://www.sciencedirect.com/science/article/pii/S0092867420304062. Acesso em: 27 nov. 2020.
LEE, Rosalind C.; FEINBAUM, Rhonda L.; AMBROS, Victor. The C. elegans heterochronic gene lin-4 encodes small RNAs with antisense complementarity to lin-14. Cell, [S.L.], v. 75, n. 5, p. 843-854, dez. 1993. Elsevier BV. http://dx.doi.org/10.1016/0092-8674(93)90529-y. Disponível em: https://www.sciencedirect.com/science/article/abs/pii/009286749390529Y. Acesso em: 24 nov. 2020.
LI, Caixia et al. Differential microRNA expression in the peripheral blood from human patients with COVID‐19. Journal Of Clinical Laboratory Analysis, [S.L.], v. 34, n. 10, p. 0-0, 22 set. 2020. Wiley. http://dx.doi.org/10.1002/jcla.23590. Disponível em: https://onlinelibrary.wiley.com/doi/10.1002/jcla.23590. Acesso em: 19 abr. 2021.
LI, Jie et al. MiR‐627/HMGB1/NF‐κB regulatory loop modulates TGF‐β1‐induced pulmonary fibrosis. Wiley: Cellular Biochemistry, [S], v. 120, n. 3, p. 2983-2993, 09 dez. 2018. Disponível em: https://onlinelibrary.wiley.com/doi/abs/10.1002/jcb.27038. Acesso em: 06 mai. 2021
LIU, Zhi et al. Implications of the virus-encoded miRNA and host miRNA in the pathogenicity of SARS-CoV-2. Cornell University, [s. l], p. 2-26, 10 abr. 2020. Disponível em: https://arxiv.org/abs/2004.04874. Acesso em: 19 abr. 2021.
LIU, Zhi et al. SARS-CoV-2 encoded microRNAs are involved in the process of virus infection and host immune response. The Journal Of Biomedical Research, [S.L.], v. 35, n. 3, p. 216, 2021. Journal of Biomedical Research. http://dx.doi.org/10.7555/jbr.35.20200154.
LUJAMBIO, Amaia; LOWE, Scott W.. The microcosmos of cancer. Nature. [S.L.], p. 347-355. 15 fev. 2012. Disponível em: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3509753/. Acesso em: 21 nov. 2020.
MASOOD, Nosheen; YASMIN, Azra. Entangling Relation of Micro RNA-let7, miRNA-200 and miRNA-125 with Various Cancers. Pathology & Oncology Research, [S.L.], v. 23, n. 4, p. 707-715, 9 jan. 2017. Springer Science and Business Media LLC. http://dx.doi.org/10.1007/s12253-016-0184-0.
MICHLEWSKI, Gracjan; CÁCERES, Javier F.. Post-transcriptional control of miRNA biogenesis. RNA: A Publication of the RNA Society. [S.L.], p. 1-16. 17 out. 2018. Disponível em: http://www.rnajournal.org/cgi/doi/10.1261/rna.068692.118. Acesso em: 21 nov. 2020.
OSÓRIO, Maria Regina Borges; ROBINSON, Wanice Mirian. Genética Humana. 3. ed. Porto Alegre: Artmed, 2013. 783 p.
PAULO ROEHE (Rio Grande do Sul). Universidade Federal do Rio Grande do Sul (ed.). Coronavírus, Covid-19, SARSCoV-2 e outros – um ponto de vista virológico. 2020. Jornal da Universidade. Disponível em: https://www.ufrgs.br/jornal/coronavirus-covid-19-sarscov-2-e-outros-um-ponto-de-vista-virologico/. Acesso em: 29 nov. 2020.
PIERCE, Jacob B. et al. Computational Analysis of Targeting SARS-CoV-2, Viral Entry Proteins ACE2 and TMPRSS2, and Interferon Genes by Host MicroRNAs. Genes, [S.L.], v. 11, n. 11, p. 1354-1254, 16 nov. 2020. MDPI AG. http://dx.doi.org/10.3390/genes11111354. Disponível em: https://www.mdpi.com/2073-4425/11/11/1354/htm. Acesso em: 27 nov. 2020.
REYES~HERRERA, Paula H.; FICARRA, Elisa. One Decade of Development and Evolution of MicroRNA Target Prediction Algorithms. Genomics, Proteomics & Bioinformatics, [S.L.], v. 10, n. 5, p. 254-263, 05 out. 2012. Elsevier BV. http://dx.doi.org/10.1016/j.gpb.2012.10.001. Disponível em: https://www.sciencedirect.com/science/article/pii/S1672022912000757. Acesso em: 27 nov. 2020.
ROBERTIS, Edward M. de; HIB, José. Biologia Celular e Molecular. 16. ed. Rio de Janeiro: Guanabara Koogan, 2014. Tradução de: Iara Gonzalez Gil e Maria de Fátima Azevedo.
SANDERS, Mark F.; BOWMAN, John L. (ed.). Análise Genética: uma abordagem integrada. São Paulo: Pearson Education do Brasil, 2014. Tradução de: Luiz Cláudio Queiroz e Daniel Vieira.
SILVA, Alexsandro Macedo; RIBEIRO NETO, Luciane Maria (org.). Biologia Molecular: métodos e interpretação. Rio de Janeiro: Roca, 2015. 254 p.
SNUSTAD, D. Peter; SIMMONS, Michael J.. Genômica. In: SNUSTAD, D. Peter; SIMMONS, Michael J.. Fundamentos de Genética. 7. ed. Rio de Janeiro: Guanabara Koogan, 2017. Cap. 15. p. 559-560.
SOLTANI, Ismael et al. Potential functions of hsa-miR-155-5p and core genes in chronic myeloid leukemia and emerging role in human cancer: a joint bioinformatics analysis. Genomics, [S.L.], v. 113, n. 4, p. 1647-1658, jul. 2021. Elsevier BV. http://dx.doi.org/10.1016/j.ygeno.2021.04.014.
SUÍÇA. World Health Organization. United Nations Organization. Painel do WHO Coronavirus Disease (COVID-19). 2020. Disponível em: https://covid19.who.int/. Acesso em: 26 nov. 2020.
UZUNIAN, Armênio. Coronavírus SARS-CoV-2 e Covid-19. Jornal Brasileiro de Patologia e Medicina Laboratorial. Rio de Janeiro, p. 0-0. 25 set. 2020. Disponível em: http://www.scielo.br/scielo.php?script=sci_arttext&pid=S1676-24442020000100051&lng=pt&nrm=iso. Acesso em: 29 nov. 2020.
VARGAS, Lúcia Rosane Bertholdo (org.). Genética Humana. São Paulo: Pearson Education do Brasil, 2014.
ZAHA, Arnaldo; FERREIRA, Henrique Bunselmeyer; PASSAGLIA, Luciane M. P. (org.). Biologia Molecular Básica. 5. ed. Porto Alegre: Artmed, 2014.






