Fungos desempenha um papel importante como constituintes de microbiota normal dos indivíduos, entretanto com as mudanças de hábitos da nova sociedade, cada vez mais, espécies que antes eram colonizadoras, possuem caraterísticas de virulência e têm preocupado bastante a comunidade médica. Estima-se que cerca de 10% destas leveduras são reconhecidas como agentes etiológicos de infecções humanas que geralmente são caracterizadas como oportunistas comensais da superfície de mucosas e pele 1.
No contexto das espécies de Candida; C. albicans representa de 60 a 90% dos isolamentos laboratoriais, C. tropicalis cerca de 7%, outras espécies como C. krusei, C. guillermondii, C. glabrata e C. parapsilosis são evidenciadas em menor frequência, porém estas são preocupantes pelo elevado número de resistência as drogas comumente utilizadas na prática clínica 2,6. Leveduras do gênero Candida estão adaptadas ao corpo humano, entretanto esta relação de equilíbrio é muito sútil, propiciada pela manutenção da integridade das barreiras teciduais, e pelo funcionamento adequado da resposta imune. Em contrapartida, estas espécies possuem fatores de virulência nas quais expressam de forma equilibrada a sua capacidade de aderência e de produção de enzimas e toxinas 4,5,6.
É sabido que a capacidade de causar doença por espécies de Candida é facilitado pela expressão de fatores associados à virulência como a capacidade de formar biofilme e a capacidade de produzir e secretar enzimas hidrolíticas, em particular proteases e fosfolipases 7. Estas enzimas facilitam a sua nutrição, adesão, colonização, invasão no epitélio humano e degradação de proteínas relacionadas ao sistema imunológico, disseminação e resistência aos medicamentos antifúngicos 7.
O primeiro processo patológico que as leveduras usam para invadir o tecido dos hospedeiros susceptíveis é a adesão às células epiteliais. Neste caso, a presença de receptores específicos na membrana citoplasmática é necessária para a fixação e penetração intracelular do fungo8. A adesão a superfície celular do hospedeiro é influenciada por fatores como a formação do tubo germinativo, disponibilidade de carboidratos, pH, temperatura, produção de fosfolipases, de proteases e de outras enzimas extracelulares 9,10.
As espécies de Candida por serem polimórficas, ou seja, elas podem se reproduzir por gemulação, dando a célula uma forma oval característica das leveduras ou podem crescer sob a forma filamentosa através da produção de tubos germinativos resultando numa conversão da forma de levedura para um crescimento em forma de micélio, com produção de hifas e pseudo-hifas 11,12,13. Esta habilidade de alternar entre a forma unicelular de levedura e a forma filamentosa é conhecida como dimorfismo13. A formação de forma micelar tem sido relacionada com o aumento da virulência em decorrência da variabilidade antigênica da superfície, conferindo uma maior aderência, dificultando a fagocitose extra e intracelular pelo sistema imune13.
Quanto a formação de enzimas citadas anteriormente (proteases e as fosfolipases), ambas atuam na destruição nas membranas celulares das células hospedeiras. As proteases desempenham um papel importante na degradação dos componentes da mucosa como o colágeno e a queratina, assim como de componentes do sistema imunológico como citosinas e anticorpos, facilitando a invasão dos tecidos do hospedeiro 13, 14. As fosfolipases degradam os fosfolipídios da membrana plasmática das células do hospedeiro, alteram as características da superfície dessas células, facilitando a aderência e consequentemente, a infecção13, 14.
A capacidade das leveduras de aderir a uma ampla variedade de superfícies inanimadas e formar biofilme em soluções glicosiladas parece protegê-las das respostas imunes do hospedeiro, bem como da ação de agentes antimicrobianos; garante as leveduras maior patogenicidade. Biofilmes patogênicos formados por espécies de Candida, sobretudo a C. albicans, C. tropicalis, C. parapsilosis e C. glabrata constituem um sério risco a vida do paciente. Pesquisas indicam que 65 a 80% das infecções microbianas são resultantes de biofilmes patogênicos, no entanto, o biofilme formado por espécies de Candida ainda não é totalmente compreendido 15.
Para a formação do biofilme, as células passam por uma fase complexa de preparo. Sendo assim, a célula-mãe do biofilme se adere a superfície livre e utiliza diversos mecanismos auxiliares para que ocorra a adesão de forma eficiente, como adesinas e interações eletrostáticas não especificas. Após essa fase, a célula passa a liberar substâncias mantedoras da adesão e início da formação de micro colônias que irão coalescer. Em seguida, tem-se o biofilme formado por estruturas do fungo, matriz polimérica, poros e canais de água que permitem o fluxo de nutrientes e metabólitos (Figura 1). O biofilme se desloca e pode liberar leveduras que têm a habilidade de se desenvolverem em condições desfavoráveis e formar novas estruturas de biofilme 13,15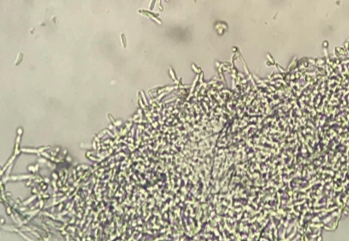 Figura 1: São evidenciadas estruturas microscópicas (matrix polimérica, filamentos micelianos, blastoconídios e clamidoconídios) do biofilme de C. albicans formado em placa de poliestireno. Fonte: Silva, G.M.
Figura 1: São evidenciadas estruturas microscópicas (matrix polimérica, filamentos micelianos, blastoconídios e clamidoconídios) do biofilme de C. albicans formado em placa de poliestireno. Fonte: Silva, G.M.
Fungos que produzem biofilmes captam nutrientes de forma mais assertiva, favorecendo um crescimento mais ordenado e na maior proteção contra radiações UV, fagocitose, desidratação e resistência a antifúngicos. Estudo que indicam os fatores de virulência de patógenos, sobretudo os de etiologia fúngica, são necessários, uma vez que espécies de Candida contribuem para agravamento do estado de saúde dos pacientes em âmbito hospitalar e causas de doenças graves como a septicemia.
Referências
- VALLE, G. C.; RENDE, J. C.; OKURA, M. H. Estudo da Incidência do Gênero Candida em Hospital Público Universitário. NewsLab. São Paulo, v.17, n.101, p. 202-222, 2010.
- SCHERMA, A. P. et al. Presença de Candida spp na cavidade bucal de lactantes durantes os primeiros quatro meses de vida. Cienc. Odontol. Bras., São José dos Campos, v.7, n. 3, p. 79-86, 2004.TAMAI IA, PAKBIN B, FASAEI BN. Genetic diversity and antifungal susceptibility of Candida albicans isolates from Iranian HIV-infected patients with oral candidiasis. BMC Res Notes. 14: 1-7. 2021.
- SEDDIKI, A. et al. Infectivités fongiques des cathéters implantés dues à Candida Formation des biofilms et résistance. J Mycol Méd. v.25, p.130-135, 2015.
- CALDERONE, R. A.; FONZIWA, W. A. Virulence factors of albicans. Trends Microbiol., Cambridge, v. 9, p. 327-335. 2001.
- COLOMBO AL, NAKAGAWA Z, VALDETARO F, BRANCHINI MLM, KUSSANO EJU, NUCCI M. Susceptibility profile of 200 bloodstream isolates of Candida spp collected from Brazilian tertiary care hospitals. Medical Mycology 41: 235-239, 2003.
- FIGUEIREDO-CARVALHO, M. H. G.; RAMOS, L. d. S.; BARBEDO, L. S.; OLIVEIRA, J. C. A. d. et al. Relationship between the antifungal susceptibility profile and the production of virulence-related hydrolytic enzymes in Brazilian clinical strains of Candida glabrata. Mediators of inflammation, 2017, 2017.
- MAGDALENA, Matta de Henning; PERRONE, Marianella. Factores determinantes de patogenicidad en relación a la ecologia de Candida albicans en cavidad bucal. Acta Odontol. Venez., Caracas, v. 39, n. 2, 2001.
- VIDOTTO, V. et al. Adherence of Candida albicans and Candida dubliniensis to bucal and vaginal cells. Rev. Iberoam. Micol., Barcelona, v.20, p. 52-54, 2003.
- KHAN, M. S. A, et al. Virulence and Pathogenicity of Fungal Pathogens with Special Reference to Candida albicans. Combating Fungal Infections. In: AHMAD, I., ET AL. Combating Fungal Infection: problems and remedy. Berlin: Springer. p.21 – 45. 2010
- GOW, N.A.R. et al. Candida albicans morphogenesis and host defense: discriminating invasion from colonization. Nat. Rev. Microbiol., Londres, v. 10, n.2, p. 112-122, 2012.
- SIDRIM & ROCHA M. Micologia Médica à Luz de Autores Contemporâneos, Guanabara Koogan, 2003
- TORTORA, Gerard J. Principios de anatomia e fisiologia. 14 ed. Rio de Janeiro: Guanabara Koogan, 2019, 1201 p
- OMBRELLA, A. M.; RAMOS, L.; RAMOS, L. Actividades proteinasa y fosfolipasa de aislamientos de Candida albicans provenientes de secreciones vaginales con distintos valores de pH. Iberoam. Micol., Barcelona, v. 25, p. 12-16, 2008.
- YU, S.B. et al. The Activities of adhesion and biofilm formation by Candida tropicalis clinical isolates display significant correlation with its multilocus sequence typing. Mycopathologia, v. 182, n. 5-6, p. 459-469, 2017.
ACESSE AGORA:
https://www.yumpu.com/pt/document/read/68093276/revista-newslab-edicao-177/94






