Autores: Yasmin Pina de Almeida e Anderson Pereira Soares.
INTRODUÇÃO
A Escherichia coli é um bacilo Gram negativo, pertencente à família Enterobacteriaceae de grande importância clínica, que em situações normais coloniza o trato gastroinstestinal de seres humanos e outros animais em uma relação de comensalismo, ou seja, de uma forma não patogênica (1, 2). Entretanto, existe uma grande variedade de sorotipos da espécie que apresentam um alto potencial de patogenicidade por possuírem importantes fatores de virulência, sendo assim capazes de provocar infecções intestinais e/ou extra intestinais, sendo denominadas como Escherichia coli diarreiogênicas (3).
A Escherichia coli Produtora de Toxina Shiga (STEC), e por vezes também denominada como Escherichia coli Enterohemorrágica (EHEC) ou ainda como Escherichia coli produtora de Verotoxina (VTEC), é uma categoria de bactérias que engloba uma grande variedade de sorotipos de microrganismos pertencentes ao grupo de Escherichia coli diarreiogênicas, cujo principal fator de virulência é a produção de citotoxinas bacterianas com alto potencial de patogenicidade: as Toxinas Shiga- Like (STx), ou por vezes denominadas Verotoxinas (VTx), que são capazes de inibir a síntese de proteínas em células e desencadear uma série de processos patológicos (4). Esses microrganismos podem produzir unicamente ou concomitantemente um ou dois tipos de toxinas Shiga: a Toxina Shiga Tipo 1 (STx1) essa que muito se assemelha à citotoxina produzida pela Shigella dysenteriae e a Toxina Shiga Tipo 2 (STx2) que não se diferenciam no mecanismo de ação, entretanto são estruturalmente e antigenicamente distintas entre si. Dentre esses tipos, a STx2 é a toxina que está mais comumente presente em quadros mais graves relacionados a infecção por STEC (5, 6). Cada um desses dois tipos da citotoxina possuem variantes que são classificadas a partir da existência de subtipos, sendo eles: STx1a, STx1b, STX1c, STx1d, STx2a, STx2b, STx2c, STx2d, STx2e, STx2f, STx2g, STx2h, STx2i, STx2j e STx2k (6), estes são estruturalmente distintos, além de diferenciar- se pelo nível de citotoxicidade, capacidade de ligação (afinidade e dissociação) ao receptor globotriacilceramida (GB3) e pelo tipo de reservatório ou espécie do hospedeiro (6, 7).
O principal reservatório para tais microrganismos é o trato gastrointestinal do gado bovino, sendo assim o consumo de alimentos de origem animal (carne, leite não pasteurizado e seus derivados), de água e vegetais que estejam contaminados pelas fezes desses animais, são potenciais e as principais fontes de transmissão dessa bactéria ao homem, não excluindo-se também a possibilidade de transmissão pessoa a pessoa via oral- fecal (8). A dose infectante deste microrganismo é relativamente baixa, visto que a ingestão de aproximadamente 100 bacilos já é o suficiente para desencadear uma infecção (9).
As manifestações clínicas desencadeadas pela ação da bactéria e pelos efeitos citotóxicos nas infecções por STEC podem evoluir e variam em grau de gravidade, tendo seu início entre 3 à 4 dias após a contaminação, com a ocorrência de uma diarreia profusa e dores abdominais, com a possibilidade de progressão para a manifestação de Colite Hemorrágica (CH), patologia que cursa com a intensificação do quadro de diarreia, aliado à presença de sangue nas fezes, que pode perdurar por até aproximadamente 5 dias (10) , e em quadros mais graves, há a possibilidade de evolução para a Síndrome Hemolítico Urêmica (SHU), uma complicação grave caracterizada pela presença de três principais indicativos clínicos: anemia hemolítica do tipo microangiopática, trombocitopenia e insuficiência renal aguda (11, 12), sendo de importância salientar que, crianças menores de 5 anos estão mais propensas ao desenvolvimento de SHU, sendo esta considerada uma das principais causas de insuficiência renal em crianças nesta faixa etária (10, 13). Além da insuficiência renal crônica ser uma possível sequela em pacientes com SHU, danos neurológicos, cardíacos e pancreáticos também são frequentemente relatados nestes casos (13, 14).
As terapias de suporte à vida e o tratamento sintomático, que incluem a reposição hídrica e eletrolítica a partir da administração endovenosa de cristaloides, suporte e monitoramento da pressão arterial, e em casos de complicações a realização de diálise, plasmaférese terapêutica, transfusão de concentrado de hemácias e de plaquetas e transplante renal, são as medidas terapêuticas mais indicadas e mais amplamente utilizadas no manejo de casos de infecção por STEC (10). A administração de antibióticos especificamente em casos de infecção por STEC é deveras controversa, sendo na maioria das vezes contraindicada, tendo em vista que algumas classes de antibióticos podem ser prejudiciais, ao induzir a um agravamento dos casos e aumentar consideravelmente o risco de desenvolvimento da Síndrome Hemolítico Urêmica (15), uma vez que por diversos mecanismos estes fármacos induzem a uma maior produção da toxina shiga pela bactéria, levando-se em consideração também, os mecanismos de ação de antimicrobianos que levam à lise das bactérias o que consequentemente, desencadeia uma maior liberação e circulação da toxina (16).
Tanto a Toxina Shiga Tipo 1 (STx1), quanto a Toxina Shiga Tipo 2 (STx2) consistem em uma estrutura proteica AB5 (figura 1) composta por uma subunidade A, que compreende o sitio ativo enzimático da citotoxina e uma subunidade B (17), que consiste no sítio de ligação da mesma ao receptor globotriacilceramida (GB3) na célula hospedeira (17), sendo este receptor expresso na superfície de células endoteliais dos rins, intestino e cérebro (18), e sendo o antígeno de diferenciação (CD77) em um tipo de específico de linfócito B (19). Na STx1, a subunidade A é composta por cerca de 315 aminoácidos e na STx2 essa mesma porção possui cerca de 319 aminoácidos; em ambos os tipos da toxina, há um sítio sensível a tripsina que permite que essa porção seja clivada em uma subunidade A1 e uma subunidade A2 estando estas ligadas a partir de uma ponte dissulfeto (10); a atividade enzimática da toxina encontra-se especificamente na subunidade A1 sendo essa a porção responsável por inibir a síntese proteica nas células hospedeiras ao ter ação enzimática atuando como uma N-glicosidase (10). Por sua vez, a subunidade B consiste em um pentâmero ligado a subunidade A2 da cadeia A por uma ligação não covalente formado por cinco subunidades menores idênticas em que cada uma destas subunidades possui aproximadamente 69 aminoácidos na STx1 e 71 aminoácidos na STx2 (5).
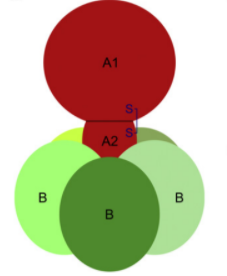
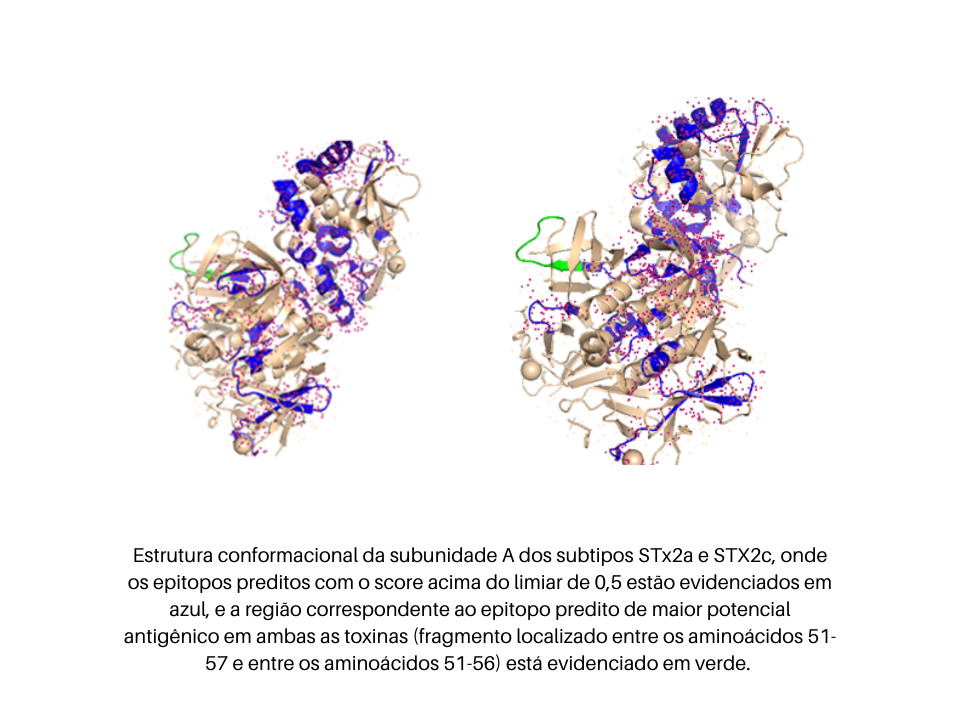
Figura 1: Estrutura comum e geral da Toxina Shiga, sendo esta formada por uma subunidade A, que ao ser clivada se divide em duas subunidades menores: A1 e A2, além de uma subunidade B que consiste em um pentâmero composto por cinco subunidades iguais (17).
A Escherichia coli produtora de Toxina Shiga e seus mais diversos sorotipos são considerados de grande relevância médica e epidemiológica por serem o agente etiológico presente em importantes surtos de origem alimentar ocorridos a partir do ano de 1982 (3, 20), em países desenvolvidos como os Estados Unidos da América, Alemanha e Japão. Na Argentina, país fronteiriço ao Brasil, os casos de infecção por STEC são endêmicos, sendo considerados um grande problema de saúde pública (21). Segundo dados mundiais da Organização Mundial de Saúde (OMS), estimasse que anualmente, ocorram entre 0,6 a 136 casos de infecções por STEC a cada 100.000 pessoas (8).
No Brasil, apesar de não haver a ocorrência de grandes surtos reportados, uma grande variedade de sorotipos desses microrganismos em específico é amplamente detectada em animais criados para o consumo humano (principalmente em bovinos) e como contaminantes em produtos alimentícios, o que representaria potenciais fontes de transmissão da bactéria à humanos (22), além da ocorrência de casos isolados em humanos (23) envolvendo sorotipos de extrema importância clínica e epidemiológica, como exemplo: O157:H7 (o sorotipo mais presente em surtos ocorridos mundialmente e o agente etiológico responsável por casos de maior gravidade) e o sorotipo O111:H8, sendo este último, o sorotipo mais frequentemente identificado no país (13, 24); No Brasil, a Escherichia coli O111:H8 tem o seu principal fator de virulência a partir da produção de Toxina Shiga tipo 1a (STx1a), por sua vez, a Escherichia coli O157:H7 possui um maior potencial patogênico ao ter a capacidade de produzir habitualmente dois dos subtipos mais patogênicos da toxina: a Toxina Shiga tipo 2a (STx2a) e a Toxina Shiga tipo 2c (STx2c) (23, 25).
Os dados epidemiológicos de casos de infecções por STEC em humanos no Brasil são desatualizados e insuficientes, o que pode ser explicado a partir do baixo emprego de métodos diagnósticos que sejam específicos e que possibilitem a identificação do sorotipo do microrganismo, o que de certa forma impossibilita a implementação de uma vigilância ativa e específica para esses casos, o que poderia evidenciar uma subnotificação de casos isolados e surtos (26). Do mesmo modo, apesar da presença deste patógeno ser constantemente evidenciada a partir do isolamento de sorotipos de STEC em alimentos, animais e em amostras humanas no país, há uma certa escassez de estudos específicos que incluam a análise estrutural in sílico dos subtipos de toxinas do tipo Shiga produzidas pelos principais sorotipos de Escherichia coli já isolados em amostras humanas no Brasil.
 LEIA O ARTIGO CIENTÍFICO NA ÍNTEGRA EM NOSSA NOVA EDIÇÃO – CLIQUE AQUI
LEIA O ARTIGO CIENTÍFICO NA ÍNTEGRA EM NOSSA NOVA EDIÇÃO – CLIQUE AQUI