Olá, nosso assunto de hoje é a persistência, conhecida entre nós como uma das qualidades dos vencedores e pessoas de sucesso.
Mas não é dos seres humanos que iremos falar, mas sim das bactérias, pois sua persistência as têm mantido vivas mesmo após ataques com antibióticos. Como isso acontece?
Pesquisadores da Universidade Surrey, Reino Unido, publicaram um estudo no The Proceedings of the National Academy of Sciences (PNAS), periódico da National Academy of Sciences do Reino Unido, intitulado “Loss of phenotypic inheritance associated with ydcI mutation leads to increased frequency of small, slow persisters in Escherichia coli”, ou “Perda da herança fenotípica associada à mutação ydcI leva a um aumento da frequência de persistências pequenas e lentas em Escherichia coli”.
Quando estamos nos referindo a bactérias, persistência não muda exatamente de conceito. Pelo contrário. Bactérias persistentes são as que sobrevivem a processos como a exposição a antibióticos.
A persistência provoca tratamentos prolongados e surgimento de resistência, e o estudo em questão visa rastrear cepas de Escherichia coli selvagens e de alta persistência.
Este conceito não é novo, ele vem de 1942, quando Gladys Hobby, e colaboradores, observou comportamento diferente em cepas de estreptococos quando submetidas à ação da Penicilina. As cepas deste estudo, sobreviveram ao tratamento, e foram denominadas “persistentes”. Posteriormente, outro pesquisador, Joseph Bigger, as chamou de “resistentes”. Notemos que estes estudos antecedem o método de Kirby e Bauer, que viria somente ao final dos anos 60 do século passado.
Após verificação de fenômenos semelhantes, este foi qualificado como “variação fenotípica”, devido ao fato das cepas persistentes serem geneticamente idênticas às cepas não resistentes. Há descrição de persistência para grande parte das bactérias patogênicas, sendo responsável por falhas terapêuticas e resistência em infecções crônicas.
O QUE AS TORNA PERSISTENTES?
Segundo os pesquisadores, a persistência está associada ao crescimento lento, e este, ao aumento de cepas em fase lenta e em fase estacionária de crescimento.
Em seu estudo, foram identificados dois tipos de persistores: o tipo I, cepas não crescentes formadas durante a fase estacionária, e o tipo II, células de crescimento lento geradas durante o crescimento exponencial, denominada por consenso como persistência espontânea, por ter surgido durante crescimento exponencial.
As cepas em questão foram caracterizadas como uma cepa mutante de E. coli de alto colesterol (Hip), particularmente uma cepa HipA7. Este fenótipo é causado pela mutação do gene que codifica uma toxina de um sistema toxina-antitoxina.
As evidências mostram que um defeito na herança fenotípica da variação da taxa de crescimento, é responsável pelo aumento da frequência de persistências, e que tal defeito tem como responsável, pelo fenótipo HipQ, o gene ydcI.
RESUMINDO O ESTUDO
O estudo demonstra que em cepas de E. coli, o fenótipo de alto índice de hipQ é causado por uma mutação no gene ydcI , que está associada ao fenótipo de herança fenotípica reduzida (RPI), fenômeno que deve ser investigado e reportado em outros gêneros e espécies bacterianas, cujo comportamento leva a crer em alta persistência, tais como cepas de Mycobacterium tuberculosis, com a qual vários pesquisadores já estão com estudos avançados, como Vicheze et al., que estabeleceram um modelo in vitro de persistência da tuberculose e micobacteriófagos, publicados no mesmo PNAS, sob o título (traduzido por nós) “A respiração aprimorada evita a tolerância e a resistência aos medicamentos no Mycobacterium tuberculosis”. O aprimoramento da respiração, através da adição de N-acetilcisteína ou vitamina C, impediu a formação de persistentes.
Há ainda estudos que demonstram que alterações no status metabólico estão relacionados à persistência, e por consequência, à taxa de crescimento, tamanho celular e crescimento assimétrico em micobactérias, assim como em E. coli.
Segundo todos estes estudos, a caracterização do vínculo entre o gene ydcI e o fenômeno RPI, poderá esclarecer os mecanismos responsáveis pela variação fenotípica, como a persistência, e poderá gerar formas de tratar infecções causadas por bactérias persistentes.
ESTAMOS VIVENDO UMA MUDANÇADE PARADIGMA?
Após a descoberta da penicilina por Alexander Fleming, o mundo passou a ter poder terapêutico contra os as infecções causadas por bactérias, um dos momentos mais importantes da história da medicina, culminando com o Prêmio Nobel ao trio Fleming, Florey e Chain.
A ampla necessidade de combater infecções, gerou uso maciço deste grupo de fármacos (antibióticos), e por sua vez, a “reação bacteriana” mediada pelo desenvolvimento de mecanismos de resistência, que foram surgindo de acordo com os lançamentos da indústria, novas drogas ao arsenal. Ocorre que, desde o início da chamada era da antibioticoterapia, a medicina utiliza o mesmo formato terapêutico, que leva em consideração a disputa “antibiótico versus bactéria”, ou seja, a resposta do microrganismo frente ao “ataque” farmacológico.
É fato, indiscutível, que a resistência bacteriana aos antibióticos seja um dos mais complexos problemas que a humanidade tem enfrentado, ou pelo menos tentado enfrentar.
Olhando para o momento, e fazendo um comparativo com o que podemos ver ao olharmos para trás, percebemos que quase nada, ou muito pouco mudou no comportamento dos profissionais envolvidos, de forma direta, com o desenvolvimento e surgimento deste fenômeno. Os erros parecem insistir em permanecer e nos levando a chegar onde chegamos.
Mas, ao mesmo tempo, a resistência bacteriana tem movimentado o meio científico – que busca formas de sucesso, porém sem êxito – que precisa repensar, e está repensando, a forma de conduzir a terapêutica antibacteriana.
Vivemos, ou viveremos afinal, uma sonhada “mudança de paradigma”?
O PARADIGMA
Após as primeiras descobertas, e os primeiros antibióticos lançados no mercado, cabia à ciência descobrir mais sobre suas eficácias terapêuticas, quando a primeira proposta de padronização de testes de determinação de perfis de sensibilidade de bactérias frente a um rol de antibióticos é publicada em 1966.
Esta proposta, que ficou conhecida como “método de Kirby & Bauer”, revolucionou o formato de análise crítica da relação entre bactérias e antibióticos, com uma técnica na qual a medição de uma zona de inibição, determina se a bactéria é sensível ou resistente ao antibiótico em teste, e nascia o “antibiograma”.
Então, chegamos ao momento da história no qual a medicina tem em mãos alguns importantes instrumentos: a cultura, o antibiograma e os antibióticos.
O provável paradigma se estabeleceu, e até os dias de hoje, iniciando o tratamento logo após a coleta das amostras, empiricamente e baseados em guidelines.
Após aguardar os resultados de identificação do agente etiológico e antibiograma, se confere se a droga escolhida, e a terapêutica afim, passa a ser (ou não) alicerçada por resultados laboratoriais, incluído decisões chamadas “descalonamentos”, quando uma droga é substituída por outra, caso não haja necessidade de seu uso, como no caso de uma cepa de S. aureus sensível à Oxaxilina em pacientes sob uso de Vancomicina.
É claro que sabemos que, na imensa maioria dos casos, isso não acontece, já que nem sempre o antibiograma é solicitado e realizado, e quando realizado, é subutilizado, sub-interpretado e, porque não dizer, muitas vezes mal executado.
Este modelo é o mesmo há cerca de setenta anos, lembrando que o antibiograma só surgiria mais de vinte anos após os primeiros antibióticos.
No ano de 1962, Thomas Samuel Kuhn, físico e filósofo norte-americano, publicou sua mais importante obra: “Estrutura das Revoluções Científicas”. Nela, Kuhn traz um novo modelo científico, que prega que “a produção do conhecimento começa com a observação neutra, se dá por indução, é cumulativa e linear, e que este conhecimento científico é definitivo”.
Baseados nos conceitos de Kuhn, podemos concluir que o modelo terapêutico antibacteriano é um paradigma?
Estaria a medicina passando, portanto, por uma mudança de paradigma?
A ideia passada por Kuhn é representada por um esquema chamado de “Ciclo de Kuhn”, que contém as etapas do raciocínio científico necessárias às avaliações de paradigmas, suas mudanças e consequências.
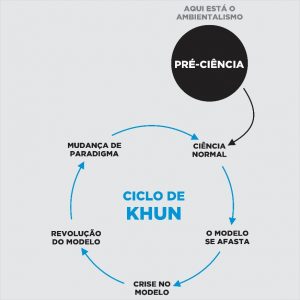
Figura 1: Ciclo de Kuhn
Todos os campos científicos passam pelo mesmo tipo de ciclo, uma espécie de ciclo comum, que começa na Pré-Ciência, momento em que há problemas, há interesses, há interessados, porém não se tem as ferramentas necessárias à capacitação científica para que se progrida no campo proposto.
Em um determinado momento, surge um “modelo orientador da compreensão”, o chamado “paradigma de campo”, quando ocorre o avanço para “ciência normal”, período de maior permanência. Neste momento, vem um afastamento do paradigma e o modelo entra em crise, sendo que para os cientistas, não serve mais como guia de resolução mesmo após inúmeras tentativas de correção para que continue servindo.
O modelo falha e quebra, iniciando o período de revolução do modelo científico, do paradigma em si. Esta etapa inicia com o surgimento de novos candidatos a modelo, e são completamente distintos do anterior, e dentre os muitos candidatos, emerge um novo conceito, um novo modelo a seguir, um novo paradigma. A mudança e o estabelecimento do novo paradigma como uma nova ciência fecha o ciclo, e estamos de volta à ciência normal, primeiro passo do ciclo que, futuramente, certamente entrará em colapso gerando a instabilidade dos modelos e surgimento de novos paradigmas.
Um fato a ser considerado é que pessoas são resistentes a mudanças, ainda mais quando essa mudança é de um modelo científico seguido há tanto tempo, e, no caso especificamente da antibioticoterapia, mais de setenta anos.
Não teria isso acontecido no decorrer da era pós surgimento da resistência?
O MODELO E A CONSEQUÊNCIA
Até pouco tempo atrás, não havia grande preocupação com resultados de cultura e antibiograma, já que o arsenal de drogas era mais do que o suficiente para combater – e vencer – as infecções causadas por bactérias.
Porém, sabe-se que, apenas quatro anos após o início do uso da penicilina pela medicina, os primeiros indícios de resistência à esta droga por bactérias do gênero Staphylococci são descritos na literatura.
Os autores demonstraram, experimentalmente, a existência de uma cepa de S. aureus vinte mil vezes mais resistente à penicilina em comparação a cepas sensíveis, buscando chamar a atenção a um problema emergente e que futuramente poderia causar falha terapêutica nos pacientes tratados com drogas deste grupo.
Outro estudo mostrava, ainda na década de 40, que algumas bactérias poderiam produzir enzimas capazes de hidrolisar o anel beta-lactâmico das penicilinas, sendo por isso denominadas “penicilinases”.
Mas as descobertas não paravam.
O primeiro relato de resistência de Staphylococcus aureus ao grupo da meticilina (Meticillin Resistant Staphylococcus aureus – MRSA) se deu em 1961, apenas dois anos após o lançamento da droga no mercado sob o nome comercial de “Celbenin”, o que traria resistência a absolutamente todos os beta-lactâmicos, incluindo os carbapenêmicos, grupo descoberto em 1976 e utilizado em massa desde 1985, sendo o grupo de antibióticos de maior espectro dentre os conhecidos, e amplamente utilizados contra bactérias resistentes a outros betalactâmicos e em infecções severas. Somente recentemente, com o lançamento das cefalosporinas anti-MRSA, essa verdade deixou de ser absoluta.
Isso se repete com as cefalosporinas, carbapenêmicos, e mais recentemente, com as polimixinas, e fatalmente ocorrerá com os demais fármacos recentemente lançados e, porque não dizer, com os futuros. O fato é que o modelo está falho.
A REFLEXÃO
O estudo demonstrado no início deste texto, mostra que há persistência nas bactérias patogênicas, e que podemos ter aí mais uma luz no fim do túnel neste relacionamento entre seres humanos e microrganismos, mas, muita coisa precisa mudar, principalmente no comportamento, seja da enfermagem, prescritores, farmacêuticos, fisioterapeutas e/ou microbiologistas.
A mudança de modelo, ou mudança de paradigma, é a meta a ser alcançada no combate aos microrganismos e as infecções por eles causadas, pois certamente, pelas consequências de nossos atos, não estamos, definitivamente, no caminho certo.
Assim como no campo terapêutico, o modelo atual de diagnóstico e tratamento está em risco, pois muitas vezes nem baseado em evidências o é. Se no global vivemos tempos de descentralização de poder de decisão, no diagnóstico – microbiológico – ainda não chegamos lá.
Atualmente, em nosso país, a política tomou o espaço da ciência. Decisões que deveriam estar sendo tomadas democraticamente, respeitando opiniões distintas, não acontecem. São tomadas arbitrariamente, e poderão trazer consequências sérias em um futuro próximo. Mas o setor parece não perceber, não interrogar. Permanecer na escuridão da passividade, permitindo que poucos decidam por nós, é um erro, pois o que parece correto, nem sempre correto é.
Cabe a nós interrogarmos sempre, e jamais devemos aceitar decisões que trarão impacto em nossos resultados, e por consequência nas escolhas clínicas, sem querer saber verdadeiramente os porquês, já que somos responsáveis pelos laudos que assinamos e liberamos, cujos serão base para decisões de alto impacto na segurança do paciente.
A mudança de paradigma está próxima, e o modelo parece estar sendo abalado o suficiente para entrar em crise. Neste momento delicado, o foco, que deveria ser buscar fortalecer ações já iniciadas há décadas, teima em permanecer em mudanças de impacto duvidoso.
Vamos nos preparar para essa quebra de paradigma, buscando entender o que fazemos, por que fazemos e para quem fazemos.
Qual é o impacto de nossos resultados nesse contexto, afinal? Quem somos nós nesta cadeia diagnóstica? Para responder, é preciso compreender, e para compreender, estudar muito e interrogar a tudo.
Portanto, estude, se especialize, e fundamentalmente, sempre interrogue, afinal, a aplicação da ciência é nosso dever, e a busca de evidências, nossa segurança e de nossos pacientes.
 Caio Salvino é farmacêutico-bioquímico, microbiologista clínico, professor e consultor. Apaixonado pela profissão que escolheu, dirige o Laboratório Saldanha, em Lages e a ImersãoLab Capacitação e Treinamentos em Análises Clínicas, em Floripa, ambas na Santa e bela Catarina. É idealizador e apresentador do talk-show Papo de Jaleco no YouTube.
Caio Salvino é farmacêutico-bioquímico, microbiologista clínico, professor e consultor. Apaixonado pela profissão que escolheu, dirige o Laboratório Saldanha, em Lages e a ImersãoLab Capacitação e Treinamentos em Análises Clínicas, em Floripa, ambas na Santa e bela Catarina. É idealizador e apresentador do talk-show Papo de Jaleco no YouTube.





