Fabiola O Paes Leme¹, Lucas Braga Costa dos Santos*²
1 Doutor, Professor, Departamento de Clínica e Cirurgia, Escola de Veterinária, Universidade Federal de Minas, Belo Horizonte, MG, Brasil.
2 Programa de pós-graduação em ciência animal, Departamento de Clínica e Cirurgia, Escola de Veterinária, Universidade Federal de Minas, Belo Horizonte, MG, Brasil.
*autor para correspondência: lucasbraga_costa@hotmail.com
Na medicina veterinária existem quatro metodologias principais para a realização das contagens diferenciais de leucócitos. A primeira é o método manual, que consiste na realização da leitura de esfregaço sanguíneo em microscópio óptico. As outras opções são baseadas em métodos automáticos, sendo elas a impedância, a citometria de fluxo e a análise quantitativa da camada flogística (Lehner et al., 2007; Denicola,2011).
As metodologias automáticas conseguem avaliar milhares de células em poucos minutos ou segundos. Essa característica permite que os equipamentos obtenham resultados com alta precisão, reduzindo consideravelmente o coeficiente de variação (CV) do teste e aumentando a sensibilidade a variações biológicas (Weiss & Wardrop, 2010).
Harvey (2012) apresentou uma comparação entre os coeficientes de variação (CV) obtidos pela contagem manual e automática (citometria de fluxo) e determinou que o CV do método automático foi significativamente menor que do método manual para todas as linhagens de leucócitos. As metodologias automáticas citadas dependem, em algum grau, da identificação do tamanho das células para a diferenciação. Essa característica cria uma limitação já que linhagens diferentes podem ter tamanhos semelhantes entre si, principalmente em animais doentes (Denicola,2011).
Os basófilos geralmente são subestimados por métodos automáticos por possuírem tamanho semelhante aos outros granulócitos, embora estejam em menor concentração no sangue. Achados de lâmina, como agregados plaquetários, podem influenciar na contagem de leucócitos, porque os agregados possuem tamanho maior que as plaquetas individuais. Condições patológicas, como leucemias podem liberar células atípicas na circulação que não serão classificadas corretamente na automação (Stockham & Scott,2011).
As metodologias automáticas também omitem informações de grande importância tanto para o diagnóstico quanto para o prognóstico. Achados de lâmina como neutrófilos tóxicos, linfócitos reativos ou atípicos, monócitos ativados, células eritróides nucleadas, inclusões intracitoplasmáticas e características morfológicas nucleares não são avaliadas pelas metodologias automáticas disponíveis atualmente (Thrall et al., 2012).
Um ponto importante sobre a contagem diferencial manual, é o mito que apenas 100 leucócitos são observados durante o processo. Um bom patologista clínico trata a leitura diferencial de um hemograma como um exame citológico, ou seja, avalia todo o esfregaço, incluindo, além da área de contagem, o corpo e a franja. Essa última, geralmente acumula uma grande quantidade de leucócitos, principalmente aqueles com alguma alteração morfológica (figura 1). Por isso, centenas, se não milhares, de células também são avaliadas em poucos minutos. Isso permite que o patologista clínico expresse sua opinião sobre aquela amostra. Essa subjetividade do exame frequentemente é bem-vinda, porque carregará a experiência do examinador e consequentemente uma grande quantidade de informações valiosas para o clínico (Santoro, 2018).
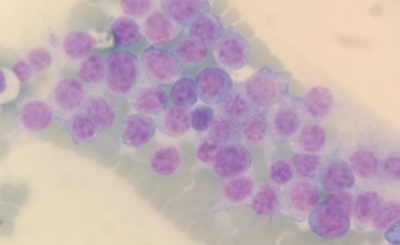
Figura 1. Franja de esfregaço sanguíneo de cão com suspeita de leucemia linfoide. Presença de concentração intensa de células linfoides atípicas. (Fonte: Laboratório de Patologia Clínica Veterinária da Escola de Veterinária da Universidade Federal de Minas Gerais)
Considerações finais
A automação da contagem diferencial nos equipamentos mais modernos, principalmente os que utilizam a técnica da citometria de fluxo, apresentam confiabilidade satisfatória para a contagem diferencial de leucócitos de cães e gatos. Contudo, a utilização da automação deve estar atrelada a um controle de qualidade rigoroso dos processos e equipamentos do laboratório. A utilização das máquinas não excluí a necessidade de avaliação do esfregaço sanguíneo por um patologista clínico, já que a identificação de alterações morfológicas celulares somente pode ser feita dessa maneira.
Referências bibliográficas
DENICOLA, D. B. Advances in Hematology Analyzers. Topics In Companion Animal Medicine, v. 26, n. 2, p. 52-61, maio 2011. Elsevier BV. http://dx.doi.org/10.1053/j.tcam.2011.02.001.
HARVEY, J. W. Veterinary Hematology: a diagnostic guide and color atlas. St. Louis: Elsevier, 2012. 360 p.
LEHNER, J.; GREVE, B.; CASSENS, U. Automation in Hematology. Transfusion Medicine And Hemotherapy, v. 34, n. 5, p. 328-339, 2007. S. Karger AG. http://dx.doi.org/10.1159/000107368.
SANTORO, P. Manual methods vs automated hematology analyzers in veterinary hematology. Veterinary Clinical Pathology, v. 47, n. 2, p. 178-178, jun. 2018. Wiley. http://dx.doi.org/10.1111/vcp.12611.
STOCKHAM, S. L.; SCOTT, M. A. Fundamentos de Patologia Clínica Veterinária. 2. ed. Rio de Janeiro: Guanabara Koogan, 2011. 729 p. Tradução Cid Figueiredo et al.
THRALL, M. A., WEISER, G., ALLISON, R. W., CAMPBELL, T. W. Veterinary Hematology and Clinical Chemistry. 2. ed. Ames: John Wiley & Sons, 2012. 762 p.
WEISS, D. J.; WARDROP, K. J. Schalm’s Veterinary Hematology. 6. ed. Ames: Blackwell Publishing, 2010. 1206 p.
*******************************************************************************************************************************
A Diagno apresenta a sua Linha Icounter de analisadores hematológicos: Icounter 5D, Icounter 3D e Icounter VET
Primeiros analisadores hematológicos 100% idealizados e produzidos no Brasil, vieram para transformar a rotina dos pequenos e médios laboratórios com mais velocidade e confiança para diagnósticos mais precisos. Possuem menu intuitivo, têm baixo consumo de reagentes e tem produção nacional, facilitando a assistência técnica e está menos vulnerável às variações cambiais, gerando maior economia. A Diagno possui uma rede de distribuidores exclusivos no Brasil, altamente capacitados para a comercialização e pós venda da linha Icounter.

Icounter 5D
Display colorido touchscreen 8”
Impressora térmica embutida
Faz até 80 análises por hora (45 segundos para um hemograma completo)
26 parâmetros: GB; LIN#; MON#; NEU#; EOS#; BAS#; LIN%; MON%; NEU%; EOS%; BAS%; GV; HGB; HCT; VCM; HCM; CHCM; RDW-CV; RDW-SD; PLT; VPM; PCT; P-LCR; P-LCC PDW-CV; PDW-SD. 2 histogramas e 1 scattergrama
Os dois princípios usados para realizar as medições são:
- O método de Impedância usado para determinar GB, GV e PLT; e medição de VCM e VPM.
- O método de Absorbância de Luz para determinar a dosagem de HGB;
- A análise das células diferenciais dos Glóbulos Brancos é feita através do método Citometria de fluxo

Icounter 3D
Display colorido touchscreen 8”
Impressora térmica embutida
Faz até 100 análises por hora (36 segundos para um hemograma completo)
24 parâmetros: GB; LIN#; MID#; NEU#; LIN%; MID%; NEU%; GV; HGB; HCT; VCM; HCM; CHCM; RDW-CV; RDW-SD; PLT; VPM; PCT; PDW-CV; PDW-SD; P-LCR; P-LCC. 3 histogramas
Os dois princípios usados para realizar as medições são:
- O método de Impedância usado para determinar GB, GV e PLT; e medição de VCM e VPM.
- O método de Absorbância de Luz para determinar a dosagem de HGB

Icounter VET
Display colorido touchscreen 8”
Impressora térmica embutida
Faz até 100 análises por hora (36 segundos para um hemograma completo)
24 parâmetros: GB, LIN#, MID#, NEU#,EOS#, LIN%, MID%, NEU%, EOS%, GV, HGB, HCT, VCM, HCM, CHCM, RDW-SD, RDW-CV, PLT, VPM, PCT, PLC-R, PLC-C, PDW-CV, PDW-SD.
Os dois princípios usados para realizar as medições no são: –
- O método de Impedância usado para determinar GB, GV e PLT; e medição de VCM e VPM.
- O método de Absorbância de Luz para determinar a dosagem de HGB
Site: diagno.ind.br
Redes sociais: @diagnobrasil
(31) 3489.5100






