RESUMO
O Sars-CoV-2 é um vírus que causa síndrome respiratória aguda e grave. O novo coronavírus foi encontrado no ano de 2019 por pesquisadores da província de Wuhan na China. O Sars- CoV-2 gera uma inflamação sistêmica levando a uma sepse grave, insuficiência respiratória e cardíaca, disfunção múltipla de órgãos e coagulopatia grave. No exame laboratorial a maioria dos pacientes apresentam linfopenia e os pacientes graves apresentam neutrófilos significativamente altos, D-dímeros também muito elevados e queda acentuada de plaquetas e fibrinogênio. Pacientes infectados com Sars-CoV-2 podem apresentar uma resposta exacerbada do sistema imune, que causa uma vasta liberação de citocinas em resposta à infecção viral e/ou infecções secundárias podendo resultar em uma tempestade de citocinas e sintomas de sepse. Completando o quadro inflamatório característico do choque séptico, pacientes acometidos pela COVID-19 apresentam um severo quadro de coagulação intravascular disseminada, que se caracteriza por um aumento de D-dímeros e parâmetros de coagulação anormal. A hipercoagulabilidade que ocorre no curso da COVID-19 é um marcador significativo para o mau prognóstico da COVID-19. Estão sendo administrados anticoagulantes nos pacientes, principalmente a heparina não fracionada (HNF) e a heparina de baixo peso molecular (HBPM). Estes dois tipos de heparinas são muito utilizadas no manejo de pacientes com a COVID-19, pois possuem propriedades anticoagulantes e antitrombóticas, esses fármacos também possuem efeitos anti-inflamatórios, citoprotetivos e antivirais. Nesta revisão, foi resumido o conhecimento atual sobre os disturbios e coagulação que acometen pacientes com COVID-19.
Palavras-chave: Sars-CoV-2; Coronavírus; COVID-19; CIVD; coagulação; hipercoagulabilidade, D-dímeros.
ABSTRACT
Sars-CoV-2 is a virus which causes acute and severe respiratory syndrome. The new coronavirus was found in 2019 by researchers from Wuhan province in China. Sars-CoV-2 generates systemic inflammation leading to severe sepsis, respiratory and cardiac failure, multiple organ dysfunction and severe coagulopathy. On laboratory examination, most patients have lymphopenia and critically ill patients have significantly high neutrophils, also very high D-dimers and a marked drop in platelets and fibrinogen. Patients infected by the Sars-CoV-2 may exhibit exacerbated immune system response, which causes a wide release of cytokines in response to viral infection and/or secondary infections that can result in a cytokine storm and symptoms of sepsis. Completing the inflammatory condition characteristic of septic shock, patients affected by COVID-19 have a severe disseminated intravascular coagulation, which is characterized by increase in D-dimers and abnormal coagulation parameters. The hypercoagulability that occurs in the course of COVID-19 is a significant marker for the poor prognosis of COVID-19. Anticoagulants are being administered to patients, mainly unfractionated heparin (UFH) and low molecular weight heparin (LMWH). These two types of heparins are widely used in the management of patients with COVID-19, as they have anticoagulant and antithrombotic properties, these drugs also have anti- inflammatory, cytoprotective and antiviral effects. In this review, the current knowledge about disorders and coagulation affecting patients with COVID-19 was summarized.
Keywords: Sars-CoV-2; Coronavirus; COVID-19; CIVD; coagulation; hypercoagulability, D-dimers.
INTRODUÇÃO
O surgimento do novo coronavírus (Sars-CoV-2) provocou uma pandemia que gerou um caos humanitário na saúde e trouxe grandes desafios para o meio científico, tanto para o diagnóstico como para o tratamento. O Sars-CoV-2 infectou milhões de vítimas ao redor do mundo, e, desde o seu descobrimento, em dezembro de 2019 até o momento atual, os números entre as vítimas só aumentam, e o grande desafio para os pesquisadores é a busca de elementos que possam esclarecer a fisiopatologia do vírus e desenvolver terapias, principalmente anticorpos, capazes de proteger a população (1).
Os sintomas da doença por Sars-CoV-2 caracterizam-se por ter variação entre os pacientes, pois pode se apresentar como uma simples gripe, assintomática até uma grave insuficiência respiratória. Os principais sintomas da infecção por Sars-CoV-2 são febre alta, tosse seca, e cansaço. Já os sintomas menos comuns são descritos como diarreia, dor de garganta, conjuntivite, perda de apetite, erupções cutâneas e descoloração das extremidades. Em adição, os sintomas graves são dispneia grave, dores no peito, perda de movimentos e da fala (1).
A partir das estatísticas, a gravidade da doença é maior na população acima de 60 anos ou que possuem doenças preexistentes como diabetes, hipertensão e asma. O diagnóstico da doença do Sars-CoV-2 (COVID-19) é feito por RT-PCR que detecta o RNA do vírus a partir da amplificação do ácido nucleico pela reação em cadeia de polimerase. Além disso, podem ser utilizados imunoensaios e teste imunocromatográficos para a detecção de anticorpos IgG e IgM para Sars-CoV-2 (2).
O Sars-CoV-2 gera uma inflamação sistêmica levando a uma sepse grave, insuficiência respiratória e cardíaca, disfunção múltipla de órgãos e coagulopatia grave. No exame laboratorial a maioria dos pacientes apresentam linfopenia e os pacientes graves apresentam neutrófilos significativamente altos, D-dímeros também muito elevados, além de ureia e creatinina também elevados, caracterizando uma insuficiência renal aguda (1).
Embora a doença associada ao Sars-CoV-2 se manifeste principalmente nos pulmões, foi demonstrado que também se manifesta em outros sistemas orgânicos. Dados clínicos e patológicos recentes demonstram uma associação entre Sars-CoV-2 e coagulopatia que podem se manifestar como embolia pulmonar (EP) ou trombose venosa, arterial e/ou microvascular, que estão associadas à lesão viral grave do endotélio pulmonar (3).
METODOLOGIA
Para a realização deste trabalho foi feito uma revisão sistemática abordando a temática “distúrbios de coagulação em pacientes com Sars-CoV-2”. Para a análise literária foram utilizados os seguintes bancos de dados: Pubmed, Scientific eletronic library online (Scielo). Ainda utilizou-se para a pesquisa os seguintes temas: Sars-CoV-2, Coagulation in COVID-19, coagulopathy in Covid-1, fibrinogen and d-dimer Sars-Cov-2, anti-coagulation covid-19, disseminated intravascular coagulation covid-19.
Os critérios de inclusão foram artigos publicados em português e inglês, com alta relevância cientifica no período de dezembro de 2019 até o presente ano contendo os descritores acima.
O VÍRUS SARS-COV-2
O Sars-CoV-2, como foi descrito pelos pesquisadores, é um vírus que causa síndrome respiratória aguda e grave. O novo coronavírus foi encontrado no ano de 2019 por pesquisadores da província de Wuhan na China. O coronavírus chamado de Sars-CoV-2 tem origem da família coronavidae da ordem nidorivirales vírus zoonóticos. Os coronavidae são classificados em quatro grupos que incluem α-coronavírus, β- coronavírus, γ- coronavírus e δ- coronavírus. Entre eles, α- e β-Coronavírus são os mais importantes para o ser humano, já que infectam mamíferos e aves, sendo que o Sars-CoV-2 pertence ao grupo β. Essa família de vírus é transmitida por contato e foi encontrado primeiramente em morcegos e transmitido entre humanos a partir da liberação de partículas expelidas do trato respiratório contaminado (2; 4).
MECANISMO DE AÇÃO DO VÍRUS
O Sars-CoV-2 é um vírus de RNA de fita simples e possui quatro proteínas estruturais as quais são proteína E (proteína de envelope), proteína M (proteína de membrana), proteína S (proteína Spike) e proteína N (nucleocapsídio) e estas proteínas estão relacionadas com a estrutura viral, regulação e função respectivamente. A proteína S atua no processo de infecção viral já a proteína N atua diretamente na formação do capsídeo e da estrutura viral (4).
O processo de infecção por Sars-CoV-2 ocorre a partir da ligação da proteína S com um receptor enzimático à enzima conversora de angiotensina 2 ECA2. O vírus se une à membrana e libera seu RNA viral no interior da célula do hospedeiro (célula humana). Após a ligação ao receptor ECA2 o vírus utiliza o mecanismo de endocitose do hospedeiro para se fundir com a membrana plasmática e internalizar-se. O vírus endocitado é transportado para o endossoma inicial, a seguir, para o endossoma tardio e, eventualmente, para o lisossomo, onde é ativado e adquire a capacidade de iniciar a replicação e infecção (5; 6; 7). A Figura 1 demonstra a estrutura do vírus.
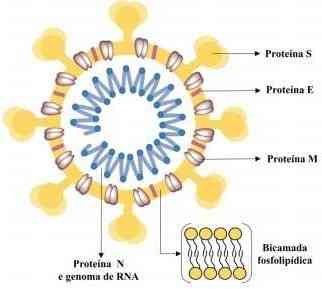
Figura 1 – Estrutura do Sars-CoV-2
Fonte: (4).
O Sars-CoV-2 e a Resposta Inflamatória
Pacientes infectados com SARS-CoV-2 podem apresentar uma resposta exacerbada do sistema imune, que causa uma vasta liberação de citocinas em resposta à infecção viral e/ou infecções secundárias podendo resultar em uma tempestade de citocinas e sintomas de sepse que são a causa da morte em 28% dos casos fatais de COVID-19 (5). A sepse é caracterizada por uma inflamação sistêmica frente a uma infecção. E essa inflamação ocorre em consequência à atividade de diversas células, tais como macrófagos, neutrófilos e linfócitos que levam à formação de estresse oxidativo, produção excessiva das redes extracelulares de DNA e liberação de citocinas, causando um desequilíbrio metabólico e, em consequência a disfunção orgânica (6). Portanto, a gravidade dos pacientes é devida não apenas à infecção viral, mas também à resposta imune do hospedeiro. Esta sepse viral é capaz de afetar diversos órgãos, tais como os rins, o fígado e os pulmões, gerando uma disfunção de múltiplos órgãos, fenômeno semelhante ao encontrado na sepse bacteriana (7). Estes eventos podem ser vistos na Figura 2.
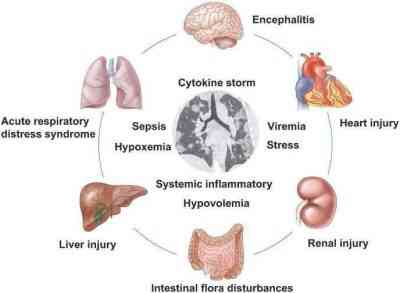
Figura 2 – Órgãos atingidos pela infecção pelo Sars-CoV-2
Fonte: (20).
Completando o quadro inflamatório característico do choque séptico, pacientes acometidos pela COVID-19 apresentam um severo quadro de coagulação intravascular disseminada, que se caracteriza por um aumento de D-dímeros, que pode atingir valores 10 ou 20 vezes maiores que os valores de referência em casos severos de infecção pelo vírus (8).
Inflamação x Coagulação
A Sepse viral é desencadeada pelo processo inflamatório gerado pela tempestade de citocinas que estimulam um processo pró-coagulante a partir da inibição da trombomodulina. A sepse viral ativa a coagulação, promovendo a expressão do fator tissular no espaço intravascular, eliminando a expressão das moléculas de adesão e leucócitos na parede vascular, diminuindo a atividade fibrinolítica e a função da via anticoagulante. A tempestade de citocinas gera um aumento significativo nos marcadores de formação de trombina, fragmentos de protrombina e complexo de trombina antitrombina, também gerando uma diminuição do fibrinogênio que faz sua conversão para fibrina (9; 12).
Sars-CoV-2 e a Hipercoagulabilidade
As células endoteliais contribuem para a preservação da homeostase por manter a parede do vaso integra e o balanço da coagulação e fibrinólise, através da expressão de inibidores da coagulação e síntese de enzimas que podem lisar o coágulo. Várias evidências estão mostrando que na COVID-19, o primeiro passo para a desestabilização do sistema de coagulação é a lesão do endotélio vascular que leva à iniciação e propagação dos efeitos desta enfermidade (9).
A hipercoagulabilidade pode ser definida por um quadro de excessiva coagulação que pode ser provocada por alguns fatores, ou doenças, tais como, câncer, inflamação ou lesões vasculares e que podem gerar a coagulação intravascular disseminada (CIVD) (Figura 3). A CIVD consiste em uma síndrome que se caracteriza pela ativação incontrolável da coagulação e frequentemente está associada à sepse. A sua fisiopatologia ainda é complexa, porém sabe- se que a deposição sistêmica de fibrina é resultado da geração de trombina, mediada pelo complexo fator tissular/fator VII ativado (FT/ FVIIa) e da inibição ou disfunção dos anticoagulantes naturais (antitrombina [AT], proteína C (PC), proteína S [PS] e inibidor da via do fator tissular). Em adição, a inibição da atividade fibrinolítica pelo aumento dos níveis inibitórios no ativador de plasminogênio do tipo 1 (PAI-1) resulta na remoção inadequada de fibrina, contribuindo, dessa forma, para a trombose da microvasculatura (10). Citocinas, principalmente a interleucina-6, têm ação central neste processo demonstrado na ordem abaixo.
A sepse, seja ela bacteriana ou viral,, ativa a coagulação, promovendo a expressão do fator tissular no espaço intravascular, eliminando a expressão das moléculas de adesão e leucócitos na parede vascular, diminuindo a atividade fibrinolítica e a função da via anticoagulante. A tempestade de citocinas gera um aumento significativo nos marcadores de formação de trombina, fragmentos de protrombina e complexo de trombina antitrombina, também gerando uma diminuição do fibrinogênio que faz sua conversão para fibrina (3; 15). Os eventos que aceleram a coagulação podem ser vistos na Figura 3.
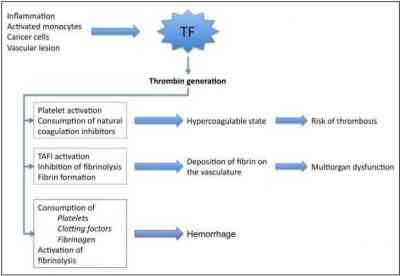
Figura 3 – Principais fatores que podem ativar o sistema de coagulação (TF-Fator tecidual)
Fonte: (16)
A hipercoagulabilidade que ocorre no curso da COVID-19 é um marcador significativo para o mau prognóstico da COVID-19. Os pacientes apresentam trombos e parâmetros de coagulação anormais tais como prolongamento do tempo de protrombina (TP) e tempo de tromboplastina parcial ativada (KTTP), aumento nos níveis de fatores de coagulação como Von Willenbrand e fator VIII da coagulação. Este quadro hematológico é característico da coagulação intravascular disseminada e está relacionado diretamente ao aumento no índice de morte dos pacientes. Na Figura 4 observa-se como as células mononucleares e as plaquetas ativadas induzem a cascata de coagulação, ativando as células inflamatórias por meio de ligação da trombina, fator tecidual e receptores específicos (11).
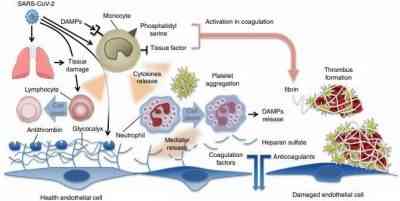
Figura 4 – Ativação da cascata de coagulação durante o processo de infecção viral pelo Sars-CoV-2
Fonte: (21)
Um importante achado clínico em pacientes graves da COVID-19 é o grande aumento de D-dímeros e uma acentuada diminuição do fibrinogênio e das plaquetas (12), conforme se observa nos exames laboratoriais de um paciente acometido por COVID-19 apresentados abaixo.
D-DÍMEROS
Material: Plasma Método: Imunoturbidimetria
Resultado: 4049,01 ng/mL Valores de referência: até 500 ng/mL
CONTAGEM DE PLAQUETAS
Material: Sangue total Método: Automação/microscopia ótica
esultado: 138.000/µL Valores de referência: 150.000 a 450.000/µL
FIBRINOGÊNIO
Material: Plasma Método: Turbidimetria
Resultado: 90 mg/dL Valores de referencia: 185 mg/dl a 400 mg/dL
Conforme se observa nas Figuras 5 e 6, os D-dímeros são produto de degradação da fibrina e quando a cascata de coagulação é acionada, a trombina é gerada de forma que culmina na conversão de fibrinogênio em monômeros de fibrina. Esses monômeros de fibrina, compostos por um dos chamados Domínio ‘E’ e dois domínios ‘D’ são estabilizados através do processo de ligação cruzada mediado pelo fator XIII ativado para formar um coágulo de fibrina insolúvel. Esta ligação cruzada é uma ligação covalente que liga irreversivelmente os domínios D de duas moléculas de fibrina adjacentes entre si. Fisiologicamente, o processo de formação do coágulo é perfeitamente equilibrado com o início simultâneo da quebra do coágulo, a chamado fibrinólise, para garantir que o lúmen do vaso sanguíneo não seja ocluído. O processo de fibrinólise é mediado via enzima plasmina, que tem a capacidade de clivar a fibrina em uma mistura heterogênea dos chamados produtos de degradação da fibrina (FDPs). A ligação covalente formada entre dois domínios D é, no entanto, resistente à degradação da plasmina. FDPs contendo dois desses domínios D são referidos como D-dímeros e são produzidos exclusivamente a partir de fibrina reticulada (13). A Figura 5 demonstra as reações de formação dos D-dímeros.
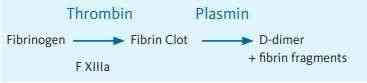
Figura 5 – Sequência de reações que dão origem aos D-dímeros
Fonte: (13).
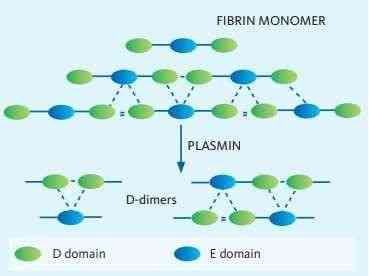
Figura 6 – Formação dos D-dímeros
Fonte: (13).
Um estudo realizado em Wuhan na China detectou que o tempo de protombina (TP) de pacientes com SARS-CoV-2 estava significativamente aumentado quando comparado com indivíduos saudáveis (81% vs 97%). O resultado mais significativo se relacionou com as concentrações dos D-dímeros, onde foram encontrados valores acima de 500 ng/mL em pacientes severamente doentes (46,4%), também 43% dos pacientes com doença leve mostraram aumento dos D-dímeros, enquanto 60% de pacientes hospitalizados em unidade de terapia intensiva mostraram um aumento significativo neste parâmetro. Além disso, vários autores relataram que a maioria dos pacientes que não sobreviveram à enfermidade tiveram níveis elevados de D-dímeros. Acredita-se que a monitorização dos D-dímeros pode ser útil no controle do curso da COVID-19 (14).
A dosagem plasmática de fibrinogênio é outro marcador importante do processo de coagulação. O fibrinogênio é uma glicoproteína de fase aguda da inflamação e integra o grupo de biomarcadores inflamatórios produzidos pelos hepatócitos e é considerado um importante marcador para acompanhar a evolução do processo inflamatório. Ele é um fator importante no processo de coagulação (fator 1), pois durante o processo de coagulação ele é transformado em fibrina. Além disso, atua na gênese do processo aterotrombótico por meio da regulação da adesão e proliferação celular, vasoconstrição no local da lesão endotelial, estimulação da agregação de plaquetas e viscosidade do sangue (15).
Apesar de ser um importante fator na coagulação, a avaliação do fibrinogênio plasmático não está sendo considerada importante na monitorização da COVID-19. Esta afirmação pode ser explicada pela seguinte questão: em pacientes com a doença pode haver uma diminuição por causa da CIVD provocada pelo vírus, entretanto, já que o fibrinogênio é uma importante molécula pró-inflamatória, ele poderá estar aumentado no sangue dos pacientes devido à tempestade de citocinas, quadro especialmente grave nos doentes em UTI (15).
As plaquetas têm um papel central no desenvolvimento das anormalidades da coagulação na sepse e podem ser ativadas diretamente por mediadores pró-inflamatórios, como o fator ativador de plaquetas, bem como por meio da trombina gerada. A ativação de plaquetas também pode estimular a formação de fibrina por mecanismo alternativo. A proteína P-selectina na membrana plaquetária que não apenas medeia a adesão de plaquetas a leucócitos e células endoteliais, mas também aumenta a expressão do fator tecidual nos monócitos. Em circunstâncias normais, a ativação da coagulação é controlada por três importantes vias anticoagulantes fisiológicas: o sistema antitrombina, o sistema ativado da proteína C, e o inibidor da via do fator tecidual. Na sepse, todas as três vias sofrem disfunção. Em meio a todo esse desbalanço do sistema de coagulação, a fibrinólise endógena é amplamente reduzida (9).
Apesar da diminuição das plaquetas representar um indicador importante na coagulação intravascular disseminada, a incidência de trombocitopenia é relativamente baixa nos pacientes com COVID 19, pois somente cerca de 45% de pacientes com diagnóstico positivo para o vírus apresentaram plaquetas abaixo de 150.000/mL (Valor de Referência: 15.000 a 450.000/µL) (13; 23; 24).
Outro dado importante com relação às plaquetas se relaciona com o fato de que alguns pacientes apresentam um aumento significativo de plaquetas (trombocitose), entretanto este achado não se reflete na gravidade da doença e esta situação paradoxal pode refletir a fase da doença. Com relação a isto é possível pensar que a trombocitopenia é provocada pelo contínuo processo de coagulação e que a trombocitose, mecanismo que não está claramente elucidado, pode ser resultado do intenso quadro inflamatório, já que as interleucinas IL-1β e IL-6 estimulam a proliferação de plaquetas, provocando a trombocitose (16).
Coagulopatia Intravascular Disseminada em Pacientes com COVID-19
A coagulação intravascular disseminada (CIVD) consiste em uma síndrome que se caracteriza pela ativação incontrolável da coagulação e frequentemente está associada à sepse.
A fisiologia da coagulopatia intravascular disseminada ainda é muito complexa; porem sabe-se que a deposição sistêmica de fibrina é resultado da geração de trombina, mediada pelo Complexo fator tissular/fator VII ativado (FT/ FVIIa) e da inibição ou disfunção dos anticoagulantes naturais (antitrombina [AT], proteína C [PC], proteína S [PS] e inibidor da via do fator tissular). Em adição, a inibição da atividade fibrinolítica pelo aumento dos níveis inibitórios no ativador de plasminogênio do tipo 1 (PAI-1) resulta na remoção inadequada de fibrina, contribuindo, dessa forma, para a trombose da microvasculatura (10). Citocinas, principalmente a interleucina-6, têm ação central neste processo (17). A Figura 7 apresenta o processo da CIVD.
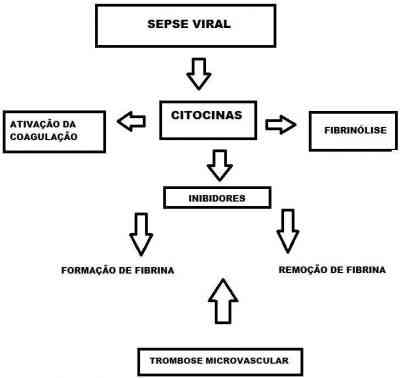
Figura 7 – Coagulação Intravascular Disseminada.
Fonte: Elaborado pela acadêmica Tusilé Soares Pinto, 2020.
Anticoagulantes como tratamento da hipercoagulabilidade em pacientes graves por COVID-19
A anticoagulação precoce foi recomendada para reduzir a trombose e a carga de microtrombos. Estão sendo administrados anticoagulantes nos pacientes, principalmente a heparina não fracionada (HNF) e a heparina de baixo peso molecular (HBPM). Estes dois tipos de heparinas são muito utilizadas no manejo de pacientes com a COVID-19, pois possuem propriedades anticoagulantes e antitrombóticas, esses fármacos também possuem efeitos anti-inflamatórios, citoprotetivos e antivirais (3).
A heparina é um polissacarídeo polianiônico sulfatado e pertence à família dos glicosaminoglicanos. A heparina interage com a antitrombina e forma um complexo que inativa várias enzimas da coagulação. A interação da heparina aumenta atividade da via intrínseca da antitrombina (17; 26).
Outros anticoagulantes com efeitos menos nocivos e de menor risco ao paciente estão sendo administrados como os anticoagulantes orais diretos (DOACs). Um destes fármacos é o Danaparoide que é um anticoagulante que funciona inibindo o fator X ativado e o fator IIa em menor proporção. Os DOACs demonstraram resultados médios em relação a pacientes internados e pós-alta com seu uso profilático. O Danaparoide demonstrou reduzir os níveis de citocinas e atenuar a trombose. Já o uso de heparina em baixas doses reduz as taxas de eventos trombóticos sem aumento de sangramento, porém, em altas taxas seus efeitos colaterais apresentam maior risco ao paciente crítico. Outro achado importante foi que pesquisas demonstram que a exposição à heparina pode reduzir infectividade do SARS-CoV- 2 e por isso, pode ser uma aliada se usada corretamente para o tratamento da doença (18).
Há muita divergência mediante o uso da heparina, já que ela pode levar a óbito caso seja administrada de maneira incorreta. Sendo assim, há necessidade de pesquisar e comparar qual melhor manejo desses anticoagulantes no tratamento, de acordo com o quadro crítico do paciente infectados por Sars-CoV-2 (19).
De acordo com critérios estabelecidos pela Sociedade Internacional de Trombose e Hemostasia (ISTH, sigla em inglês), é possível identificar melhores desfechos clínicos nos pacientes com coagulopatia intravascular disseminada recebendo terapia anticoagulante. O uso de anticoagulantes, sobretudo nos pacientes em estado crítico, não é isento de riscos e pode estar relacionado a complicações hemorrágicas graves. Portanto, a indicação dessa modalidade terapêutica deve ser personalizada, respeitando os perfis de risco trombótico e hemorrágico (9).
A terapêutica anticoagulante pode ser iniciada após o diagnóstico de coagulopatia intravascular disseminada em pacientes com a COVID-19 apesar dos riscos de hemorragia que pode ser um efeito colateral da terapêutica com anticoagulantes. Além disso, a evidência nos estudos atuais sugere o uso rotineiro da anticoagulação, principalmente em pacientes com níveis mais elevados de D-dímeros (12).
CONCLUSÃO
Este trabalho trouxe como ênfase os distúrbios hematológicos e de coagulações desencadeadas pela infecção severa provocada pelo Sars-CoV-2 que desenvolve uma sepse viral com consequente aumento dos fatores de coagulação, D-dímeros, diminuição de plaquetas e fibrinogênio, provocando uma hipercoagulabilidade que evolui para a coagulopatia intravascular disseminada.
Também durante esta revisão bibliográfica, foi abordada a eficácia do uso de anticoagulantes, enfatizando a heparina, e suas divergências sobre sua utilização como tratamento anticoagulante em pacientes críticos da COVID-19 já que seu uso ainda precisa ser pesquisado mais criteriosamente para que não haja riscos fatais ao ser administrado no paciente, como todos os outros medicamentos que já foram indicados para tratamento desta doença que acometeu tantas vítimas no mundo em tão pouco tempo.
A infecção pelo vírus Sars-CoV-2 se mostrou extremamente complexa diante dos pesquisadores, por isso necessita-se o desenvolvimento de mais estudos e evidências científicas para a doença ser tratada com dinamismo e para que haja a diminuição significativa no número de óbitos e de vítimas da doença.
REFERÊNCIAS
- Guo Y, Cao QD, Hong Z , Tan YY, Chen SD, Jin HJ, et al. The origin, transmission and clinical therapies on coronavirus disease 2019 (COVID-19) outbreak – an update on the status. Military Medical Research, v. 7, n. 1, p. 1-10,
- Naqvi AAT, Fatima K, Mohammad T, Fatima U, Singh IK, Singh A, et al. Insights into SARS-CoV-2 genome, structure, evolution, pathogenesis and therapies: Structural genomics approach. Biochimica et Biophysica Acta (BBA)-Molecular Basis of Disease, p. 165878, 2020.
- Kipshidze N, Dangas G, White CJ, Kipshidze N, Siddiqui F, Lattimer CR, et al. Viral Coagulopathy in Patients With COVID-19: Treatment and Care. Clinical and Applied Thrombosis/Hemostasis, v. 26, p. 1076029620936776, 2020.
- Lima MLSO, Almeida RKS, Fonseca FSA , Gonçalves CCS. A química dos saneantes em tempos de COVID-19: você sabe como isso funciona? Química Nova, v. 43, n. 5, p. 668-678, 2020.
- Zhang JJ, Dong X, Cao Y, Yuan Y, Yang Y, Yan Y, et al. Clinical characteristics of 140 patients infected with SARS‐CoV‐2 in Wuhan. Allergy, 75(7):1730-1741,
- Hotchkiss RS, Moldawer LL, Opal SM, Reinhart K, Turnbull IR, Vincent JL. Sepsis and septic shock. Nature reviews Disease primers, v. 2, n. 1, p. 1-21,
- Siqueira-Batista R, Gomes AP, Calixto-Lima L, Vitorino RR, Perez MCA, Mendonça EG, et al. Sepse: atualidades e perspectivas. Revista Brasileira de Terapia Intensiva, v. 23, n. 2, p. 207-216, 2011.
- Li J, Fan JG. Characteristics and Mechanism of Liver Injury in 2019 Coronavirus Disease. Journal of Clinical and Translational Hepatology, v. 8, n. 1, p. 13,
- Li H, Liu L, Zhang D, Xu J, Dai H, Tang N, et SARS-CoV-2 and viral sepsis: observations and hypotheses. The Lancet, 95(10235), p. 1517–20, 2020.
- Nascimento JHP, Gomes BFO, Carmo Júnior PR, Petriz JLF, Rizk SI, Costa IBSS, et al. COVID-19 e Estado de Hipercoagulabilidade: Uma Nova Perspectiva Terapêutica. Arquivos Brasileiros de Cardiologia, v. 114, n. 5, p. 829-833,
- Pintão MCT, Franco RF. Coagulação intravascular disseminada. Medicina (Ribeirão Preto), v. 34, n. 3/4, p. 282-291, 2001.
- Kasinathan G, Sathar J. Haematological manifestations, mechanisms of thrombosis and anti-coagulation in COVID-19 disease: A review. Ann Med Surg (Lond). 56, p. 173-177, 2020.
- Iba T, Levy JH, Levi M, Thachil J. Coagulopathy in COVID-19. Journal of Thrombosis and Haemostasis, v. 18, n. 9, p. 2103-2109,
- Hayiroglu Mİ, Cinar T, Tekkin A. Fibrinogen and D-dimer variances and anticoagulation recommendations in Covid-19: current literature review. Revista da Associação Médica Brasileira, v. 66, n. 6, p. 842-848,
- Munster M. Sysmex Educational Enhancement and Development. [Online].; 2012. Disponível em: https://www.sysmex- mea.com/fileadmin/media/f100/SEED/The role_of_the_D- dimer_test_in_clinical_diagnostics.pdf. Acesso em: 04 Set.
- Han H, Yang L, Liu R, Liu F, Wu KL, Li J, et al. Prominent changes in blood coagulation of patients with SARS-CoV-2 infection. Clinical Chemistry and Laboratory Medicine (CCLM). 58(7):1116-1120,
- Azevedo AF, Cantalice ASC, Gonzaga NC, Simões MOS, Guimarães ALV, Carvalho DF, et al. Fibrinogênio: marcador de risco cardiometabólico em crianças e adolescentes obesos ou com sobrepeso. Jornal de Pediatria, v. 91, n. 5, p. 464-470,
- Lippi G, Plebani M, Henry BM. Thrombocytopenia is associated with severe coronavirus disease 2019 (COVID-19) infections: a meta-analysis. Clinica Chimica Acta. 506: 145- 148, 2020.
- Levi M. COVID-19 coagulopathy vs disseminated intravascular coagulation. Blood advances, v. 4, n. 12, p. 2850-2850, 2020.
- Bikdeli B, Madhavan M , Gupta A, Jimenez D, Burton JR, Der Nigoghossian C, et al. Global COVID-19 Thrombosis Collaborative Group. Pharmacological Agents Targeting Thromboinflammation in COVID-19: Review and Implications for Future Research. Thrombosis and haemostasis, v. 120, n. 7, p. 1004,
- Thachil J, Tang N, Gando S, Falanga A, Cattaneo M, Levi M, et al. ISTH interim guidance on recognition and management of coagulopathy in COVID-19. Journal of Thrombosis and Haemostasis, v. 18, n. 5, p. 1023-1026,
- Sathler PC. Hemostatic abnormalities in COVID-19: A guided review. Anais da Academia Brasileira de Ciências, v. 92, n. 4,
- Weaver LK, Behrens EM. Weathering the storm: improving therapeutic interventions for cytokine storm syndromes by targeting disease pathogenesis. Current treatment options in rheumatology, v. 3, n. 1, p. 33-48, 2017.
- Giannis D, Ziogas IA, Gianni P. Coagulation disorders in coronavirus infected patients: COVID-19, SARS-CoV-1, MERS-CoV and lessons from the past. Journal of Clinical Virology, p. 104362, 2020.
- Nile SH, Nile A, Qiu J, Li L, Jia X, Kai G. COVID-19: Pathogenesis, cytokine storm and therapeutic potential of interferons. Cytokine Growth Factor Rev., 56: p. 66-70,
- Buijsers B, Yanginlar C, Maciej-Hulme ML, Mast Q, van der Vlag J. Beneficial non- anticoagulant mechanisms underlying heparin treatment of COVID-19 patients. EBioMedicine, v. 59, p. 102969,
- Hoffmann M, Kleine-Weber H, Schroeder S, Krüger N, Herrler T, Erichsen S, et al. SARS-CoV-2 Cell Entry Depends on ACE2 and TMPRSS2 and Is Blocked by a Clinically Proven Protease Inhibitor. Cell, 181(2): p. 271-280,
- Yang X, Yu Y, Xu J, Shu H, Xia J, Liu H, et al. Clinical course and outcomes of critically ill patients with SARS-CoV-2 pneumonia in Wuhan, China: a single-centered, retrospective, observational stud. The Lancet Respiratory Medicine, 8(5): p. 475-481, 2020.
- Papageorgiu C, Jourdi G, Adjambri E, Walborn A, Patel P, Fareed J, et al. Disseminated Intravascular Coagulation: An Update on Pathogenesis, Diagnosis, and Therapeutic Strategies. Clinical and Applied Thrombosis/Hemostasis, v. 24, n. 9_suppl, p. 8S-28S, 2018.
AUTORES:
Tusilé Soares Pinto1; Jarbas Rodrigues de Oliveira2
1 Formanda do Curso de Bacharelado em Biomedicina, Pontifícia Universidade Católica do Rio Grande do Sul, Porto Alegre, RS.
2 Farmacêutico, professor Doutor do Curso de Bacharelado em Biomedicina, Pontifícia Universidade Católica do Rio Grande do Sul, Porto Alegre, RS.
* Autor correspondente: Jarbas Rodrigues de Oliveira. Telefone: (51) 3320 – 3513
Endereço: Avenida Ipiranga 6681, Prédio 40, 9º andar. Porto Alegre, RS, CEP 90619-900, Brasil. E-mail: jarbas@pucrs.br






